Karbapenemlerin
Gram-Negatif Patojenlere Karşı İn Vitro Aktivitelerinin Karşılaştırmalı Değerlendirmesi:
COMPACT Çalışması Türkiye Verisi*
Comparative
Evaluation of In Vitro Activities of Carbapenemes Against Gram-Negative
Pathogens:
Turkish Data of COMPACT Study
Volkan
KORTEN1, Güner SÖYLETİR1, Ata Nevzat YALÇIN2,
Dilara ÖĞÜNÇ2, Başak DOKUZOĞUZ3,
Harika ESENER3, Sercan ULUSOY4, Alper TÜNGER4,
Bilgehan AYGEN5, Bülent SÜMERKAN5,
Dilek ARMAN6, Murat DİZBAY6, Murat AKOVA7,
Gülşen HASÇELİK7, Haluk ERAKSOY8,
Seniha BAŞARAN8, İftihar KÖKSAL9, Gülçin BAYRAMOĞLU9,
Halis AKALIN10, Melda SINIRTAŞ10
1 Marmara Üniversitesi Tıp Fakültesi, İstanbul.
1 Marmara University Faculty of Medicine, Istanbul, Turkey.
2 Akdeniz Üniversitesi Tıp Fakültesi, Antalya.
2 Akdeniz University Faculty of Medicine, Antalya, Turkey.
3 SB Ankara Numune Eğitim ve Araştırma Hastanesi, Ankara.
3 Ankara Numune Training and Research Hospital, Ankara, Turkey.
4 Ege Üniversitesi Tıp Fakültesi, İzmir.
4 Ege University Faculty of Medicine, Izmir, Turkey.
5 Erciyes Üniversitesi Tıp Fakültesi, Kayseri.
5 Erciyes University Faculty of Medicine, Kayseri, Turkey.
6 Gazi Üniversitesi Tıp Fakültesi, Ankara.
6 Gazi University Faculty of Medicine, Ankara, Turkey.
7 Hacettepe Üniversitesi Tıp Fakültesi, Ankara.
7 Hacettepe University Faculty of Medicine, Ankara, Turkey.
8 İstanbul Üniversitesi İstanbul Tıp Fakültesi, İstanbul.
8 Istanbul University Istanbul Faculty of Medicine, Istanbul, Turkey.
9 Karadeniz Teknik Üniversitesi Tıp Fakültesi, Trabzon.
9 Karadeniz Technical University Faculty of Medicine, Trabzon, Turkey.
10 Uludağ Üniversitesi Tıp Fakültesi, Bursa.
10 Uludag University Faculty of Medicine, Bursa, Turkey.
* Bu çalışma, 3. Türkiye EKMUD Kongresi (12-16 Mayıs 2010, Ankara)’nde poster olarak sunulmuştur.
ÖZET
Bu çalışmada, doripenem, imipenem ve meropenemin gram-negatif klinik izolatlara karşı in vitro aktivitesinin değerlendirilmesi amaçlanmıştır. Türkiye genelinde toplam 10 merkezden Eylül-Aralık 2008 tarihleri arasında, yoğun bakım ünitesi (YBÜ) ve YBÜ dışı hastalardan, toplam 596 adet klinik izolat toplanmıştır. Bunlardan %42.4’ü nozokomiyal pnömoni, %40.4’ü kan dolaşımı enfeksiyonu ve %17.1’i komplike intraabdominal enfeksiyon kaynaklı olup; %51.8’i YBÜ hastalarından alınmıştır. İzolatların %49.8’i Pseudomonas spp., %40.3’ü Enterobacteriaceae ve %9.9’u diğer gram-negatif etkenlerden oluşmaktadır. Her merkezde Etest® (AB Biodisk, Solna, İsveç) kullanılarak tüm izolatlar için doripenem, imipenem ve meropenemin minimum inhibitör konsantrasyonu (MİK) belirlenmiştir. İzolatlardan 188 (%31.5)’i en az bir karbapeneme dirençli bulunmuştur. Pseudomonas türlerine karşı doripenem için MİK50 değerleri meropeneme benzer olarak 1 mg/L bulunurken, imipenemden iki kat daha düşük olduğu izlenmiştir. Pseudomonas aeruginosa izolatlarının duyarlılıkları, doripenem için MİK 2 mg/L düzeyinde %64, imipenem ve meropenem için MİK 4 mg/L düzeyinde sırasıyla %53.9 ve %63 olarak tespit edilmiştir. Doripenem ve meropenem, Enterobacteriaceae türlerine karşı benzer aktivite gösterirken (MİK90 0.12 mg/L), imipenem dört kat daha az aktif (0.5 mg/L) bulunmuştur. Büyük çoğunluğunu Acinetobacter türlerinin oluşturduğu diğer gram-negatif basiller için doripenem MİK50 değeri 8 mg/L, diğer iki ilaç için ise 32 mg/L’dir. P.aeruginosa izolatları 8 mg/L MİK düzeyinde doripenem ile %84.2, meropenem ile %72.1 oranında inhibe olmuştur. Sonuç olarak doripenem, bu çalışmada toplanan patojenlere karşı genel olarak meropenem ile benzer ya da daha iyi; imipenemden ise belirgin olarak daha iyi in vitro aktiviteye sahiptir. Üç karbapenem arasında Pseudomonas türlerine karşı en aktif olan ilacın doripenem olduğu görülmüştür. Doripenem ve meropenem Enterobacteriaceae türlerine karşı benzer aktiviteye sahip olup, imipenemden en az dört kat daha aktiftir. Bu bulgular ışığında, hastanede YBÜ’de ya da YBÜ dışında tedavi gören nozokomiyal pnömoni, kan dolaşımı enfeksiyonu ve intraabdominal enfeksiyonu olan hastalar ile antibiyotik direnci gelişim riski olan hastaların antimikrobiyal tedavisinde doripenemin öne çıkan yeni bir antibiyotik olduğu kanısına varılmıştır.
Anahtar sözcükler: Karbapenem; doripenem; in vitro aktivite; gram-negatif patojen.
ABSTRACT
The aim of this study was to determine the in vitro activities of doripenem, imipenem, and meropenem against clinical gram-negative isolates. A total of 596 clinical isolates were obtained from intensive care unit (ICU) and non-ICU patients in 10 centers over Turkey between September-December 2008. The origin of the isolates was patients with nosocomial pneumonia (42.4%), bloodstream infections (%40.4), and complicated intraabdominal infections (17.1%). Of the isolates, 51.8% were obtained from ICU patients. The study isolates consisted of Pseudomonas spp. in 49.8%, Enterobacteriaceae in 40.3%, and other gram-negative agents in 9.9%. The minimum inhibitory concentrations (MIC) for doripenem, imipenem and meropenem were determined for all isolates in each center using Etest® strips (AB Biodisk, Solna, Sweden). Of the isolates, 188 (31.5%) were resistant to at least one of the carbapenems. MIC50 of doripenem against Pseudomonas spp. was 1 mg/L which was similar to that of meropenem and two-fold lower than imipenem. Susceptibility to carbapenems in P.aeruginosa was 64% for doripenem at an MIC level of 2 mg/L, 53.9% and 63% for imipenem and meropenem at an MIC level of 4 mg/L, respectively. Doripenem and meropenem showed similar activity with the MIC90 of 0.12 mg/L whereas imipenem was four-fold less active at 0.5 mg/L. Against other gram-negative pathogens, mostly Acinetobacter spp., MIC50 was 8 mg/L for doripenem and 32 mg/L for other two carbapenems. P.aeruginosa isolates were inhibited 84.2% with doripenem and 72.1% with meropenem at the MIC level of 8 mg/L. Doripenem generally showed similar or slightly better activity than meropenem and better activity than imipenem against pathogens collected in this study. Against Pseudomonas spp., doripenem was the most active of the three carbapenems. Doripenem and meropenem were equally active against Enterobacteriaceae and at least four-fold more active than imipenem. It was concluded that doripenem seemed to be a promising agent in the treatment of nosocomial pneumonia, blood stream infections and intraabdominal infections particularly in patients who were under risk of developing antimicrobial resistance.
Key words: Carbapenem; doripenem; in vitro activity; gram-negative pathogen.
Geliş Tarihi (Received): 14.10.2010 • Kabul Ediliş Tarihi (Accepted): 10.11.2010
GİRİŞ
Hastane ortamında gözlenen antibiyotik direnci, hastalarda tedavi sonucunu olumsuz etkileyebilen ve son yıllarda artış gösteren önemli bir klinik sorundur1,2. Gram-negatif patojenlere karşı direnç özellikle artmıştır ve bu dirence karşı bilinen tedavi rejimleri etkisiz kalmaktadır3. Bu patojenler arasında ciddi nozokomiyal enfeksiyonlara neden olan Pseudomonas aeruginosa, Enterobacteriaceae ve Acinetobacter türlerine karşı yaygın direnç gelişimi bildirilmiştir1,3. Hastane ortamında gözlenen antibiyotik direnci için en önemli risk faktörlerinden biri yetersiz, uygunsuz ya da uzamış antibiyotik tedavisidir. Buna engel olmak için ciddi hastane enfeksiyonlarına neden olan patojenlere yönelik akılcı bir antibiyotik politikası izlenmesi, mevcut ajanların duyarlılık profillerine uygun olarak yeterli doz ve sürede kullanılması gereklidir.
Karbapenemler, geniş spektrumlu aktiviteye sahip beta-laktam antibiyotiklerdir4,5,6. Antimikrobiyal aktivite spektrumunda gram-pozitif ve gram-negatif aerop ve anaerop patojenler bulunmaktadır5. Bu nedenle karbapenemler, tedavisi zor patojenler tarafından oluşturulan ciddi enfeksiyonların ampirik tedavisinde tercih edilmektedir. Farklı antimikrobiyal aktiviteye sahip çok sayıda karbapenemin geliştirilmesi nedeniyle artık karbapenemler homojen bir antibiyotik sınıfı olarak kabul edilmemektedir5,6. Mevcut sınıflamaya göre aerop ve anaerop patojenlere karşı etkin, ancak anti-psödomonal etkisi olmayan ertapenem, grup 1 karbapenem olarak sınıflanmıştır5,7. Bu aktivite profili ile ertapenem, hastaneye başvuran toplum kökenli enfeksiyonu olan hastaların tedavisinde önerilmektedir. İmipenem, meropenem, panipenem, biapenem ve doripenem ise grup 2 karbapenemleri oluşturmaktadır. Grup 2 ajanlar Acinetobacter spp. ve P.aeruginosa gibi non-fermentatif gram-negatif patojenleri de kapsayan geniş spektrumlu aktiviteye sahiptir ve nozokomiyal enfeksiyonların tedavisinde kullanılmaktadır6. Grup 3, metisiline dirençli Staphylococcus aureus’a karşı aktivitesi olan ajanlar için oluşturulmuştur, ancak henüz bu gruptaki ajanlardan kliniğe sunulmuş bir üye bulunmamaktadır. Grup 2 olarak sınıflanan ve yeni bir karbapenem olan doripenem, nozokomiyal pnömoni, komplike intraabdominal ve idrar yolu enfeksiyonlarının tedavisinde kullanılmaktadır. Doripenem, in vitro olarak birçok gram-pozitif, Enterobacteriaceae ve anaerop patojenler dahil olmak üzere geniş bir etki spektrumuna sahiptir8. Doripenem, Enterobacteriaceae üyelerine karşı meropenem ile benzer, Pseudomonas türlerine karşı ise artmış antimikrobiyal aktivite gösterirken, imipenem ve ertapenemden daha aktiftir8,9.
Türkiye’nin de aralarında bulunduğu 16 ülkede yürütülen COMPACT (The Comparative Activity of Carbapenem Testing Study) çalışması ile karbapenemlerin karşılaştırmalı aktiviteleri test edilmektedir10. Bu çalışmanın amacı; doripenem, imipenem ve meropenemin gram-negatif klinik izolatlara karşı in vitro aktivitesini değerlendirmektir. Burada COMPACT çalışmasına ait Türkiye verisi sunulmaktadır.
GEREÇ ve YÖNTEM
Türkiye genelinde toplam 10 merkezden Eylül-Aralık 2008 tarihleri arasında, komplike intraabdominal enfeksiyonu, bakteriyemi ya da nozokomiyal pnömonisi (ventilatörle ilişkili pnömoni dahil) olan yoğun bakım ünitesi (YBÜ) hastalarından ve YBÜ dışı hastalardan izole edilen, merkez başına 60 gram-negatif izolat (30 P.aeruginosa, 24 Enterobacteriaceae, 6 Acinetobacter spp. ve diğer gram-negatif bakteriler) çalışmaya alındı.
Çalışmaya katılan merkezler; Marmara Üniversitesi Tıp Fakültesi, Ege Üniversitesi Tıp Fakültesi, Hacettepe Üniversitesi Tıp Fakültesi, Erciyes Üniversitesi Tıp Fakültesi, Uludağ Üniversitesi Tıp Fakültesi, SB Ankara Numune Eğitim ve Araştırma Hastanesi, İstanbul Üniversitesi İstanbul Tıp Fakültesi, Akdeniz Üniversitesi Tıp Fakültesi, Gazi Üniversitesi Tıp Fakültesi ve Karadeniz Teknik Üniversitesi Tıp Fakültesi idi.
Her merkezde Etest® (AB Biodisk, Solna, İsveç) kullanılarak tüm izolatların doripenem, imipenem ve meropeneme karşı duyarlılıkları, minimum inhibitör konsantrasyonu (MİK) saptanarak belirlendi. Tüm izolatlar, tür konfirmasyonu ve sınırlı duyarlılık testi için referans laboratuvara (Quotient Bioresearch Ltd) iletildi. Bunun için merkezlerde Etest sonucuna göre doripenem, imipenem ve/veya meropenemden herhangi birine dirençli olan tüm izolatlar ile dirençli olmayan izolatların %10’u kalite kontrol testi için rastgele seçildi ve doripenem, imipenem ve meropenem için MİK değerleri “Clinical and Laboratory Standards Institute (CLSI)” tarafından önerilen sıvı mikrodilüsyon yöntemi11,12 ve Etest® ile değerlendirildi. Direnç değerlendirmesinde imipenem ve meropenem için CLSI duyarlılık sınırı, doripenem için “Food and Drug Administration (FDA)” duyarlılık sınırı kullanıldı.
İzolatların tür dağılımı, merkezlere göre direnç durumu sayı ve yüzde ile ifade edildi. Tüm hastalar, ayrıca YBÜ’de yatan ve YBÜ dışı hastalardan elde edilen izolatlar için doripenem, imipenem ve meropenemin MİK değerleri %50, %90, minimum ve maksimum olarak mg/L cinsinden verildi. Farklı patojenlere karşı doripenem, imipenem ve meropenemin kümülatif MİK dağılım eğrileri karşılaştırmalı olarak çizildi.
BULGULAR
Çalışmaya, Türkiye’den katılan 10 merkezden toplam 596 adet uygun izolat dahil edilmiştir. Bunlardan %42.4’ü nozokomiyal pnömoni, %40.4’ü kan dolaşımı enfeksiyonu ve %17.1’i komplike intraabdominal enfeksiyon kaynaklı olup; %51.8’i YBÜ hastalarından alınmıştır. İzolatların 297 (%49.8)’sinde Pseudomonas spp., 240 (%40.3)’ında Enterobacteriaceae ve 59 (%9.9)’unda diğer gram-negatif patojenler üretilmiştir (Tablo I). En sık izole edilen Enterobacteriaceae üyeleri Escherichia coli (tüm izolatların %19.3’ü), Klebsiella spp. (%14.9) ve Enterobacter spp. (%3.0)’dir.
İzolatlardan 188 (%31.5)’i en az bir karbapeneme dirençli bulunmuştur. Direnç oranı en yüksek olan merkez Erciyes Üniversitesi Tıp Fakültesi iken (%40.7), en düşük direnç oranı SB Ankara Numune Eğitim ve Araştırma Hastanesinden bildirilmiştir (%23.2) (Tablo II).
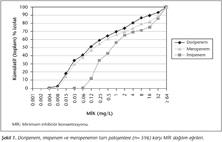
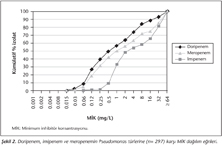
Tüm patojenlere karşı her üç karbapenem için MİK aralığı benzer bulunmuştur. Doripenem MİK50 (0.12 mg/L) değeri meropenem MİK50 (0.25 mg/L) değerinden iki kat, imipenem MİK50 (1 mg/L) değerinden sekiz kat daha düşüktür. Tüm patojenlere karşı, imipenem ve meropenem (MİK90 ≥ 64 mg/L) ile karşılaştırıldığında, doripenem en düşük MİK90 (32 mg/L) değerine sahiptir. Doripenemin tüm patojenlere karşı MİK dağılım eğrisi meropenem eğrisinden hafifçe, imipenem eğrisinden ise belirgin olarak daha soldadır (Şekil 1). Pseudomonas türlerine karşı doripenem için MİK50 değerleri meropeneme benzer olarak 1 mg/L bulunurken, imipenemden iki kat daha düşüktür. Pseudomonas türlerine karşı doripenem için MİK90 32 mg/L, imipenem ve meropenem için ≥ 64 mg/L’dir (Tablo III). Doripenemin Pseudomonas türlerine karşı MİK dağılımları meropenemden hafifçe, imipenemden ise 4-8 kat daha düşüktür (Şekil 2).
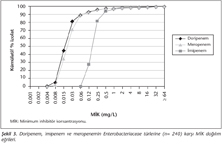
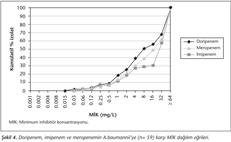
Doripenem ve imipenem Enterobacteriaceae’ya karşı benzer aktivite gösterirken (MİK90= 0.12 mg/L), imipenem dört kat daha az aktif bulunmuştur (0.5 mg/L) (Tablo III, Şekil 3). Büyük çoğunluğunu Acinetobacter’in oluşturduğu diğer gram-negatifler için doripenem MİK50 değeri 8 mg/L, diğer iki ilaç için ise 32 mg/L olarak tespit edilmiştir (Tablo III). Diğer gram-negatiflere karşı üç karbapenemin de MİK90 değeri ≥ 64 mg/L’dir (Tablo III). Acinetobacter baumannii’ye karşı MİK dağılım eğrisi her üç karbapenem için de benzer olup, MİK90 değeri her üçü için de ≥ 64 mg/L’dir (Şekil 4).
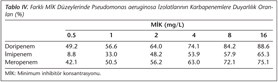
Farklı MİK düzeylerinde P.aeruginosa izolatlarının karbapenemlere duyarlılık oranları Tablo IV’te sunulmuştur. P.aeruginosa için doripenem CLSI duyarlılık sınırı belirlenmemiş, FDA tarafından ≤ 2 mg/L olarak belirtilmiştir. İmipenem ve meropenem için CLSI duyarlılık sınırı ise ≤ 4 mg/L’dir. Bu duyarlılık sınırlarına göre P.aeruginosa duyarlılıkları doripenem için %64, imipenem için %53.9, meropenem için %63 olarak tespit edilmiştir. P.aeruginosa izolatları 8 mg/L MİK düzeyinde doripenem ile %84.2, meropenem ile %72.1 oranında inhibe olmuştur.
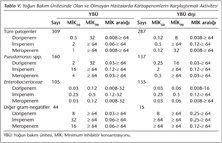
YBÜ ve YBÜ dışı hastalardan alınan izolatlar karşılaştırıldığında; tüm patojenlere (MİK90 sırasıyla 32 mg/L ve 8 mg/L), Pseudomonas türlerine (MİK90 sırasıyla 32 mg/L ve 16 mg/L) ve Enterobacteriaceae’ya (MİK90 sırasıyla 0.12 mg/L ve 0.06 mg/L) karşı doripenemin YBÜ dışı hastalarda iki kat daha aktif olduğu görülmüştür (Tablo V).
TARTIŞMA
Bu çalışmada, yatan hastalarda ciddi enfeksiyonlara sıklıkla neden olan patojenlerin karbapenemlere duyarlılığına ilişkin mevcut bilgi birikimini genişletmek amacıyla yürütülen COMPACT çalışmasına ait Türkiye verileri sunulmuştur. Elde edilen bulgulara göre doripenem Enterobacteriaceae’ya karşı meropenem ile benzer aktivite gösterirken, imipenemden daha aktif bulunmuştur. Büyük çoğunluğunu Acinetobacter türlerinin oluşturduğu diğer gram-negatifler için doripenem, diğer iki karbapenemden daha aktiftir. Pseudomonas türlerine karşı en aktif olan karbapenem ise doripenemdir.
Hastane enfeksiyonlarına neden olan bakterilerde direnç gelişimi; özellikle YBÜ’de tedavi gören, uzun süre hastanede kalan, ileri yaşta olan, girişimsel cihaz uygulanan, immünsüpresif tedavi alan ve daha önce antibiyotik kullanmış hastalar için çok önemli bir klinik sorundur3. 1990’lı yıllarda hastane kökenli antibiyotik direncinde gram-pozitif patojenler sorumlu tutulmuş, bu patojenlere karşı etkili ajanlar geliştirilmiştir. Diğer taraftan gram-negatif patojenlere karşı sınırlı sayıda yeni antibiyotik geliştirilmiştir13,14. Ancak sık görülen nozokomiyal enfeksiyonlardan (hastane kökenli pnömoni, ventilatörle ilişkili pnömoni, üriner sistem enfeksiyonu, abdominal enfeksiyonlar vb.) daha ziyade gram-negatif patojenler sorumludur15. Bu süreçte, gram-negatif patojenlerin antibiyotik direncinde artış ortaya çıkmıştır1,16. Türkiye’den yapılan bir çalışmada, YBÜ hastalarında ‰22.6 oranında ventilatörle ilişkili pnömoni bildirilmiş, en sık izole edilen etkenler Acinetobacter spp. ve P.aeruginosa olup, mevcut antibiyotiklerin çoğuna yüksek oranda direnç görülmüştür17. Bu önemli sorunun çözümü için, gram-negatiflere karşı etkili antibiyotiklerin geliştirilmesi ve yeni geliştirilenlerin duyarlılık profillerinin belirlenmesi gereklidir.
Antibiyotik duyarlılık çalışmalarına ait veriler, dirençli mikroorganizmaların kontrol altına alınması için önemli kaynak oluşturmaktadır13. Bu çalışmalardan elde edilen veriler doğrultusunda ampirik antibiyotik tedavisinin doğru planlanması mümkün olmaktadır. Özellikle ulusal ölçekli duyarlılık verileri, hekimlere antibiyotik seçiminde yol göstericidir. Bu gerekçe ile gram-negatif patojenlerin karbapenemlere duyarlılığına ilişkin veri elde etmek amacıyla yürütülen COMPACT çalışmasının Türkiye verisi, ülkemizde hastane enfeksiyonları ile mücadele eden hekimlere önemli bir kaynak sağlayacaktır.
Karbapenemler, gram-pozitif, gram-negatif ve anaerop bakterilere karşı geniş spektrumlu aktiviteye sahip beta-laktam antibiyotiklerdir6. Diğer taraftan karbapenemler Enterococcus faecium, metisiline dirençli S.aureus ve Stenotrophomonas maltophilia’ya karşı etkili değildir. İlk geliştirilen karbapenemlerden olan imipenem, dehidropeptidaz-1 (DHP-1) enzimine duyarlı olup, silastatin gibi DHP-1 inhibitörüyle verilmesi gerekirken, meropenem, ertapenem ve doripenem gibi daha yeni geliştirilenler DHP-1’e dirençlidir6. Bunlar arasında doripenem, faz III klinik çalışmalarda meropenemle benzer olarak komplike intraabdominal ve idrar yolu enfeksiyonları ile nozokomiyal pnömoni ve ventilatörle ilişkili pnömoni tedavisinde etkili olan ümit verici yeni bir ajandır8,9,18,19 ve meropeneme göre P.aeruginosa ve A.baumannii’ye in vitro aktivitesi daha fazladır6,9. Ayrıca, doripenemin in vitro olarak P.aeruginosa’ya direnç oluşturma potansiyeli, meropenem ve imipeneme göre daha düşük bulunmuştur20,21. Doripenemin, imipenem-silastatine göre santral sinir sistemi yan etkileri daha düşüktür ve daha iyi bir güvenlik profiline sahiptir22. Preklinik çalışmalarda imipenem ve meropenemden farklı olarak konvülziyona yol açma potansiyelinin olmadığı bildirilmiştir22. Doripenemin vücut dışındaki sıvılardaki stabilitesi, dört saatlik infüzyonlarla verilmesine olanak sağlamaktadır. İmipenem stabil olmadığından uzun infüzyonlara uygun değildir; meropenem ise daha kısa süreli infüzyonlarla verilebilmektedir. Uzamış infüzyonlar, beta-laktam ajanların etkinliği ile korele olan MİK üzerindeki zamanı uzatarak ilacın klinik etkinliğini artırmaktadır. Doripenem dört saatlik infüzyonla verildiğinde; 500 mg dozda 4 mg/L, 1000 mg dozda 8 mg/L düzeyinde azalmış duyarlığı olan patojenlerde doz aralığının % 40’ında MİK üzerinde kalabilmeyi sağlamaktadır23,24. Bu özellikleriyle doripenem, komplike bakteriyel hastane enfeksiyonlarının tedavisinde ilk seçenek ajanlardan biri olarak kabul edilmektedir9.
Sunulan çalışmada, YBÜ ya da YBÜ dışı kaynaklı enfeksiyon etkeni (nozokomiyal pnömoni, kan dolaşımı enfeksiyonu, komplike intraabdominal enfeksiyon) olan toplam 596 klinik izolat (Pseudomonas spp., Enterobacteriaceae ve gram-negatif basiller) üzerinde doripenemin in vitro aktivitesi diğer karbapenemlerden imipenem ve meropenem ile karşılaştırmalı olarak değerlendirilmiştir. Tüm patojenlere karşı genel değerlendirmede MİK dağılımına göre doripenemin meropenemden hafifçe, imipenemden ise belirgin olarak aktif olduğu görülmüştür. Pseudomonas türlerine karşı en aktif karbapenem ise, MİK90 değerine ve dağılım eğrisine göre doripenemdir. P.aeruginosa duyarlılıkları doripenem için MİK 2 mg/L düzeyinde %64, imipenem ve meropenem için MİK 4 mg/L düzeyinde sırasıyla %53.9 ve %63 olarak bulunmuştur. P.aeruginosa izolatları, 4 mg/L MİK düzeyinde doripenemle %74.1, meropenemle ise %63 oranında inhibe olurken; 8 mg/L MİK düzeyinde doripenemle %84.2, meropenemle ise %72.1 oranında inhibe olmaktadır. Uzamış infüzyonla verildiğinde, önerilen dozlarda standart yoldan verilen meropeneme göre farmakokinetik-farmakodinamik duyarlılık sınırlarında yaklaşık %10 daha fazla Pseudomonas suşunun doripenem ile inhibe olabileceği görülmektedir. Bu değerlerin klinikte bir fark yaratıp yaratmayacağı ilerideki çalışmaların konusudur. Enterobacteriaceae’ya karşı ise doripenem ve meropenem benzer aktivite gösterirken, imipenem dört kat daha az aktif bulunmuştur. Büyük çoğunluğunu Acinetobacter’in oluşturduğu diğer gram-negatiflere karşı üç karbapenemin de MİK90 değeri ve MİK dağılım eğrisi benzerdir. Elde edilen bu bulgular, literatürdeki karbapenemlerin gram-negatif patojenlere in vitro duyarlılık çalışmalarının verileriyle uyum içindedir. Yakın zamanda Amerika Birleşik Devletleri’nden Pillar ve arkadaşları tarafından, 12.581 klinik izolat üzerinde doripenemin in vitro aktivitesi, imipenem ve meropenem ile karşılaştırmalı olarak sıvı mikrodilüsyon yöntemiyle değerlendirilmiştir25. Bu çalışmada doripenem gram-pozitif patojenlere karşı meropenem ve imipenem ile benzer aktivitede, Enterobacteriaceae’ya karşı meropenem ve imipenemle eşit ya da daha aktif bulunurken, P.aeruginosa’ya karşı en aktif karbapenem olarak gösterilmiştir25. Yapılan diğer bir çalışmada, “Doripenem Surveillance Programme” ile doripenem ve diğer karbapenemlerin gram-negatif patojenlere karşı in vitro aktiviteleri 14.979 izolat üzerinde değerlendirilmiş, P.aeruginosa’ya karşı doripenem, imipenem ve meropenemden iki kat daha aktif; Acinetobacter türlerine karşı ise imipenem diğer karbapenemlerden hafifçe daha aktif bulunmuştur26. Bu çalışmada ≤ 2 mg/L duyarlılık sınır değeriyle P.aeruginosa izolatlarının duyarlılık oranları %85 ile en yüksek Kuzey Amerika’da, %67 ile en düşük Latin Amerika’da bildirilmiştir26. Doripenemin diğer karbapenemler ile karşılaştırmalı olarak Enterobacteriaceae’ya karşı in vitro duyarlılığının 36.614 klinik izolat üzerinde değerlendirildiği çok merkezli çalışmada da, doripenem MİK ≤ 0.5 mg/L düzeyinde Enterobacteriaceae türlerini %98.7 oranında inhibe etmiştir27.
Çalışmamızda ayrıca YBÜ ve YBÜ dışı hastalardan alınan izolatlar karşılaştırıldığında, tüm patojenlere, Pseudomonas türlerine ve Enterobacteriaceae üyelerine karşı doripenemin YBÜ dışı hastalarda iki kat daha aktif olduğu bulunmuştur. Sonuç olarak; mevcut literatür bilgisiyle uyumlu olarak doripenemin, bu çalışmada toplanan patojenlere karşı genel olarak meropenemle benzer ya da daha iyi; imipenemden ise belirgin daha iyi aktiviteye sahip olduğu saptanmıştır. Üç karbapenem arasında Pseudomonas türlerine karşı en aktif olan doripenemdir. Doripenem ve meropenem Enterobacteriaceae türlerine karşı benzer aktiviteye sahip olup, imipenemden en az dört kat daha aktiftir. Bu bulgular doğrultusunda, hastanede YBÜ’de ya da YBÜ dışında tedavi gören nozokomiyal pnömoni, kan dolaşımı enfeksiyonu ve intraabdominal enfeksiyonu olan ve antibiyotik direnci gelişimi riski altında olan hastaların antimikrobiyal tedavisinde doripenemin öne çıkan yeni bir antibiyotik olduğu görülmektedir.
KAYNAKLAR
- Slama TG. Gram-negative antibiotic resistance: there is a price to pay. Crit Care 2008; 12(Suppl 4): S4. [Özet] [Tam Metin] [PDF]
- Patel GP, Crank CW. Gram-negative resistance in the intensive care unit. J Pharm Practice 2005; 18(2): 91-9.
- Siegel RE. Emerging gram-negative antibiotic resistance: daunting challenges, declining sensitivities, and dire consequences. Respir Care 2008; 53(4): 471-9. [Özet] [PDF]
- Nicolau DP. Carbapenems: a potent class of antibiotics. Expert Opin Pharmacother 2008; 9(1): 23-37. [Özet]
- Shah PM. Parenteral carbapenems. Clin Microbiol Infect 2008; 14(Suppl 1): S175-80. [Özet]
- Zhanel GG, Wiebe R, Dilay L, et al. Comparative review of the carbapenems. Drugs 2007; 67(7): 1027-52. [Özet]
- Hammond ML. Ertapenem: a group 1 carbapenem with distinct antibacterial and pharmacological properties. J Antimicrob Chemother 2004; 53(Suppl 2): S7-9. [Özet] [PDF]
- Keam SJ. Doripenem: a review of its use in the treatment of bacterial infections. Drugs 2008; 68(14): 2021-57. [Özet]
- Dedhia HV, McKnight R. Doripenem: position in clinical practice. Expert Rev Anti Infect Ther 2009; 7(5): 507-14. [Özet]
- Morrissey I, Rossolini GM, Bouza E, et al. In vitro activity of doripenem, imipenem and meropenem against contemporary gram-negative pathogens circulating in twelve countries. 49. Interscience Conference on Antimicrobial Agents and Chemotherapy (ICAAC). September 12-15, 2009. San Francisco, USA. Poster No. E-178.
- Clinical and Laboratory Standards Institute. Performance standards for antimicrobial susceptibility testing. Seventeenth Informational Supplement. CLSI Document M100-S17, CLSI, 2007, Wayne, Pennsylvania.
- Clinical and Laboratory Standards Institute. Methods for dilution antimicrobial susceptibility tests for bacteria that grow aerobically. Approved Standard, 7th ed. NCCLS Document M7-A7. CLSI, 2006, Wayne, Pennsylvania.
- Paterson DL. Impact of antibiotic resistance in gram-negative bacilli on empirical and definitive antibiotic therapy. Clin Infect Dis 2008; 47(Suppl 1): S14-20. [Özet] [Tam Metin] [PDF]
- Rice LB. Challenges in identifying new antimicrobial agents effective for treating infections with Acinetobacter baumannii and Pseudomonas aeruginosa. Clin Infect Dis 2006; 43(Suppl 2): S100-5. [Özet] [Tam Metin] [PDF]
- Gaynes R, Edwards JR; National Nosocomial Infections Surveillance System. Overview of nosocomial infections caused by gram-negative bacilli. Clin Infect Dis 2005; 41(6): 848-54. [Özet] [Tam Metin] [PDF]
- Arya SC, Agarwal N, Agarwal S. Emerging gram-negative antibiotic resistance: daunting challenges, declining sensitivities, and dire consequences. Respir Care 2008; 53(12): 1749-50. [PDF]
- Erdem I, Ozgultekin A, Sengoz Inan A, et al. Incidence, etiology, and antibiotic resistance patterns of gram-negative microorganisms isolated from patients with ventilator-associated pneumonia in a medical-surgical intensive care unit of a teaching hospital in Istanbul, Turkey (2004-2006). Jpn J Infect Dis 2008; 61(5): 339-42. [Özet] [PDF]
- Matthews SJ, Lancaster JW. Doripenem monohydrate, a broad-spectrum carbapenem antibiotic. Clin Ther 2009; 31(1): 42-63. [Özet]
- Lucasti C, Jasovich A, Umeh O, Jiang J, Kaniga K, Friedland I. Efficacy and tolerability of IV doripenem versus meropenem in adults with complicated intra-abdominal infection: a phase III, prospective, multicenter, randomized, double-blind, noninferiority study. Clin Ther 2008; 30(5): 868-83. [Özet]
- Mushtaq S, Ge Y, Livermore DM. Doripenem versus Pseudomonas aeruginosa in vitro: activity against characterized isolates, mutants, and transconjugants and resistance selection potential. Antimicrob Agents Chemother 2004; 48(8): 3086-92. [Özet] [Tam Metin] [PDF]
- Sakyo S, Tomita H, Tanimoto K, Fujimoto S, Ike Y. Potency of carbapenems for the prevention of carbapenem-resistant mutants of Pseudomonas aeruginosa: the high potency of a new carbapenem doripenem. J Antibiot (Tokyo) 2006; 59(4): 220-8. [Özet] [PDF]
- Horiuchi M, Kimura M, Tokumura M, Hasebe N, Arai T, Abe K. Absence of convulsive liability of doripenem, a new carbapenem antibiotic, in comparison with beta-lactam antibiotics. Toxicology 2006; 222(1-2): 114-24. [Özet]
- Bhavnani SM, Hammel JP, Cirincione BB, Wikler MA, Ambrose PG. Use of pharmacokinetic-pharmacodynamic target attainment analyses to support phase 2 and 3 dosing strategies for doripenem. Antimicrob Agents Chemother 2005; 49(9): 3944-7. [Özet] [Tam Metin] [PDF]
- Van Wart SA, Andes DR, Ambrose PG, Bhavnani SM. Pharmacokinetic-pharmacodynamic modeling to support doripenem dose regimen optimization for critically ill patients. Diagn Microbiol Infect Dis 2009; 63(4): 409-14. [Özet]
- Pillar CM, Torres MK, Brown NP, Shah D, Sahm DF. In vitro activity of doripenem, a carbapenem for the treatment of challenging infections caused by gram-negative bacteria, against recent clinical isolates from the United States. Antimicrob Agents Chemother 2008; 52(12): 4388-99. [Özet] [Tam Metin] [PDF]
- Castanheira M, Jones RN, Livermore DM. Antimicrobial activities of doripenem and other carbapenems against Pseudomonas aeruginosa, other nonfermentative bacilli, and Aeromonas spp. Diagn Microbiol Infect Dis 2009; 63(4): 426-33. [Özet]
- Mendes RE, Rhomberg PR, Bell JM, Turnidge JD, Sader HS. Doripenem activity tested against a global collection of Enterobacteriaceae, including isolates resistant to other extended-spectrum agents. Diagn Microbiol Infect Dis 2009; 63(4): 415-25. [Özet]
İletişim (Correspondence):
Prof. Dr. Volkan Korten,
Marmara Üniversitesi Tıp Fakültesi,
Enfeksiyon Hastalıkları Anabilim Dalı,
İstanbul, Türkiye.
Tel (Phone): +90 212 327 4142,
E-posta (E-mail): korten@tnn.net