Pozitif Sinyal Veren Kan Kültürü Şişelerinde EUCAST Doğrudan
Hızlı Antimikrobiyal Duyarlılık Testi Yönteminin Değerlendirilmesi
Evaluation of EUCAST Direct Rapid Antimicrobial Susceptibility
Test Method in Blood Culture Bottles with Positive Signal
Gizem ERDOĞAN , Ayşe Esra KARAKOÇ , Mihriban YÜCEL , Serap YAĞCI
Ankara Eğitim ve Araştırma Hastanesi, Tıbbi Mikrobiyoloji Kliniği, Ankara.
Ankara Training and Research Hospital, Clinic of Medical Microbiology, Ankara, Turkey.
Makale Atıfı:Erdoğan G, Karakoç AE, Yücel M, Yağcı S. Pozitif sinyal veren kan kültürü şişelerinde EUCAST doğrudan hızlı antimikrobiyal duyarlılık testi yönteminin değerlendirilmesi. Mikrobiyol Bul 2021;55(4):626-634.
ÖZ
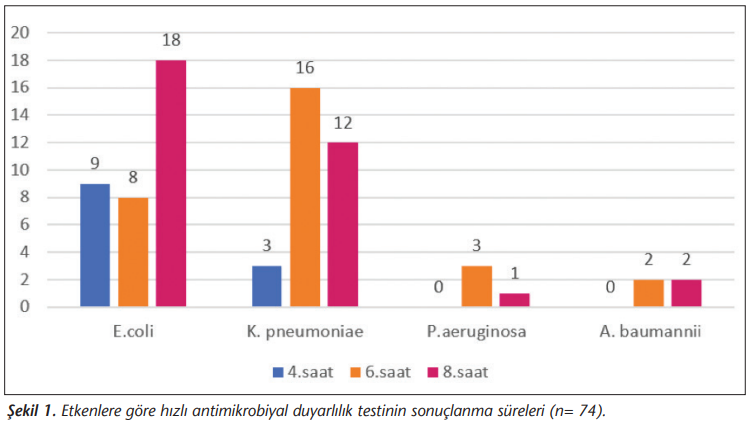
Sepsis hastalarının sağkalım şansı için antibiyotik duyarlılık testi (ADT) sonuçlarının mümkün olan en kısa sürede raporlanması esastır. “European Committee on Antimicrobial Susceptibility Testing (EUCAST)” 2019’da pozitif kan kültürü şişelerinden hızlı antimikrobiyal duyarlılık testi (HADT) yöntemiyle maksimum sekiz saat içinde antimikrobiyal duyarlılığı tespit etmek için bir öneri yayımlamıştır. Bu çalışmada BacT/ALERT (bioMérieux, Fransa) cihazında pozitif sinyal veren, Gram boyama ile gram-negatif bakteri saptanan kan kültürü şişelerinde EUCAST HADT yönteminin değerlendirilmesi amaçlanmıştır. Bu çalışma, Nisan 2019 ve Kasım 2019 tarihleri arasında prospektif olarak gerçekleştirilmiştir. Gram boyama ile aynı morfolojide gram-negatif bakteri görülen 90 kan kültürü şişesinde EUCAST HADT yöntemi uygulanmıştır. Aynı kan kültürü şişelerinden elde edilen izolatlar, EUCAST disk difüzyon yöntemi ve Vitek 2 Compact (bioMerieux, Fransa) otomatize sistemiyle çalışılmıştır. HADT ile elde edilen sonuçlar, her iki yöntemle elde edilen sonuçlarla karşılaştırılmıştır. HADT yöntemiyle antimikrobiyal duyarlılık testinin sonuçlanma süresi kaydedilmiştir. HADT yönteminin konvansiyonel yöntemlerle olan kategorik uyumu ve çok büyük hata oranları belirlenmiştir. EUCAST HADT yönteminin kapsamadığı 14 izolatın 12’si diğer Enterobacterales üyesi ve ikisi diğer non-fermentatif olarak saptanmıştır. Bir kan kültürü şişesinden yapılan Gram boyamada aynı morfolojik özellik gösteren ve antibiyogramında aynı duyarlılık profili saptanan iki farklı izolat tespit edilmiştir. Bu 16 izolat çalışma kapsamı dışında tutulmuştur. Çalışma kapsamında değerlendirilen izolatlardan 31’i Klebsiella pneumoniae, 35’i Escherichia coli, dördü Acinetobacter baumannii ve dördü Pseudomonas aeruginosa olan 74 izolatın duyarlılığı EUCAST sınır değer tablolarına göre belirlenmiştir. EUCAST HADT belirlenme sürelerine göre; E.coli için dördüncü saatte dokuz (%12), altıncı saatte sekiz (%11), sekizinci saatte 18 (%24); K.pneumoniae için dördüncü saatte üç (%4), altıncı saatte 16 (%21), sekizinci saatte 12 (%16); P.aeruginosa için altıncı saatte üç (%4), sekizinci saatte bir (%1); A.baumannii için altıncı saatte iki (%2) ve sekizinci saatte iki (%2) izolatın duyarlılık profili belirlenmiştir. HADT yönteminin otomatize sistem ile kategorik uyumu %91.8; disk difüzyon yöntemiyle %96.8 bulunmuştur. HADT yönteminde çok büyük hata, otomatize sistemle karşılaştırıldığında piperasilin-tazobaktam (%17.7), seftazidim (%11.6) ve meropenemde (%5,6); disk difüzyon yöntemiyle karşılaştırıldığında ise sefotaksim (%5.7) ve meropenemde (%6.7) saptanmıştır. EUCAST HADT sonuçlarımız, bu yöntemin düşük test maliyetiyle, hızlı sonuç vermek amacıyla kolayca rutin laboratuvarlarda uygulanabileceğini ve çok büyük hataların varlığı, sonuçların standart yöntemlerle doğrulanması gerektiğini göstermiştir.
Anahtar kelimeler: EUCAST hızlı antimikrobiyal duyarlılık testi; kan kültürü; gram-negatif bakteri.
ABSTRACT
Early reporting of the antibiotic susceptibility testing (AST) results is essential for the survival of sepsis patients. In 2019, European Committee on Antimicrobial Susceptibility Testing (EUCAST) published a proposal to detect antimicrobial susceptibility from positive blood culture bottles with a rapid antimicrobial susceptibility test (RAST) method in a maximum of eight hours. In this study, it was aimed to evaluate the EUCAST RAST method in blood culture bottles that resulted with positive signal in BacT/ALERT (bioMérieux, France) blood culture system and that showed gram-negative bacteria with single morphology with Gram stain. The study was conducted prospectively between April 2019 and November 2019. Ninety blood culture bottles that we detected single gram negative bacteria morphology by Gram stain were tested according to the EUCAST RAST method, The isolates obtained from the blood culture bottles were studied with the EUCAST disk diffusion method and the Vitek 2 Compact (bioMerieux, France) automated system. The results obtained with RAST were compared with the results of these methods. The turn around time of the RAST method was recorded. Categorical agreement of the RAST method with conventional methods and the very major error rates were determined. Of the 14 isolates not yet covered by the EUCAST HADT method, 12 were determined to be other Enterobacterales members and two as other non-fermentatives. Two isolates were detected with the same morphological characteristics in Gram stain of the blood culture bottle and the same antibiotic susceptibility profile, but with different identification results. These sixteen isolates were excluded from the study. In this study the susceptibility of 74 isolates were determined according to the EUCAST breakpoint tables, of which 31 were Klebsiella pneumoniae, 35 were Escherichia coli, four were Acinetobacter baumannii and four were Pseudomonas aeruginosa. According to the evaluation periods of EUCAST RAST; the susceptibility profile was reported for nine (12%) of E.coli at four hours, eight (11%) at six hours, 18 (24%) at eight hours; three (4%) of K.pneumoniae at four hours, 16 (21%) at six hours, 12 (16%) at eight hours; three of P.aeruginosa (4%) at six hours, one (1%) at eight hours; two of A.baumannii (2%) at six hours and two (2%) at eight hours.The categorical aggrement of the RAST method was 91.8% with the automated system and 96.8% with the disc diffusion method. Very major errors of RAST method compared to the automated system were detected for piperacillin-tazobactam (17.7%), ceftazidime (11.6%) and meropenem (5.6%); and when compared to the disc diffusion method, for cefotaxime (5.7%) and meropenem (6.7%). Our results have shown that EUCAST RAST method can practicaly be performed in routine laboratories to report early results with a low cost. Because of the very major errors it is necessary to confirm the results with the standard methods.
Keywords: EUCAST rapid antimicrobial susceptibility test; blood culture; gram-negative bacteria.
Geliş Tarihi (Received): 10.02.2021 - Kabul Ediliş Tarihi (Accepted):25.07.2021
GİRİŞ
Sepsis yaşamı tehdit eden ciddi bir klinik sorundur ve dünya çapında her yıl yaklaşık altı milyon insan sepsis nedeniyle ölmektedir. Sepsis tanısında altın standart yöntem kan kültürüdür. Sepsisli hastaların, uygun antibiyotiklerle erken tedavi edilmeleri sağkalım oranlarını arttırmaktadır. Kan kültüründe tespit edilen mikroorganizmaların antimikrobiyal duyarlılıklarının erken raporlanması, hastanın sağkalımı açısından kritik öneme sahiptir.
Disk difüzyon yöntemi, antimikrobiyal duyarlılık testinde klinik mikrobiyoloji laboratuvarlarında en yaygın kullanılan ve en eski yöntemlerden biridir. Sık rastlanan bakteriyel patojenlerin çoğunu özel bir ekipmana gereksinim duyulmadan test etmeye uygundur. “The European Committee on Antimicrobial Susceptibility Testing (EUCAST)” disk difüzyon yöntemi standart bir yöntemdir ancak bir antibiyotik duyarlılık testi (ADT) profili elde etmek için 16-24 saat gerekir. EUCAST, 2019’da pozitif kan kültürü şişelerinden hızlı antimikrobiyal duyarlılık testi (HADT) yöntemiyle maksimum sekiz saatte antimikrobiyal duyarlılık saptama önerisi yayımlamıştır[1].
Bu çalışmada, pozitif sinyal veren ve şişeden yapılan Gram boyamada aynı morfolojiye sahip gram-negatif bakteri tespit edilen kan kültürü şişelerinde EUCAST HADT yönteminin değerlendirilmesi amaçlanmıştır.
GEREÇ ve YÖNTEM
Bu çalışma, Nisan 2019-Kasım 2019 tarihleri arasında prospektif olarak gerçekleştirildi.
BacT/ALERT (bioMérieux, Fransa) cihazında pozitif sinyal veren kan kültürü şişelerinden alınan örneklerde Gram boyamada aynı morfolojik yapıdaki gram-negatif bakteriler çalışmaya dahil edildi. Tekrarlayan üremelerde ilk izolat çalışmaya alındı.
EUCAST HADT önerilerine göre seyreltilmemiş kan kültürü buyyonundan 120 μl Mueller-Hinton agara doğrudan ekim yapıldı. Piperasilin-tazobaktam (30-6 μg), sefotaksim (5 μg), seftazidim (10 μg), imipenem (10 μg), meropenem (10 μg), amikasin (30 μg), gentamisin (10 μg), siprofloksasin (5 μg), levofloksasin (5 μg), tobramisin (10 μg), trimetoprim-sulfametoksazol (1.25-23.75μg), sefotaksim (30 μg) +/- klavulonik asit (10 μg) ve seftazidim (30 μg) +/- klavulonik asit (10 μg) kombine diskleri kullanıldı. Aerobik ortamda, 35 ± 2C’de inkübe edilen plaklar dördüncü, altıncı ve sekizinci saatlerde EUCAST HADT sınır değer tablolarına göre değerlendirildi[1],[2]. Genişlemiş spektrumlu beta-laktamaz (GSBL) ve karbapenemaz varlığının tespiti için, EUCAST HADT 2019 versiyon 1.0 tarama önerilerine göre değerlendirme yapıldı.
Aynı kan kültürü şişelerinden koyun kanlı agar, EMB agar ve çikolata agar besiyerlerine ekim yapıldı. Uygun koşullarda 16-24 saatlik inkübasyon sonrası elde edilen üremelerde identifikasyon Vitek 2 Compact (bioMerieux, Fransa) otomatize sistemiyle, antimikrobiyal duyarlılık testi ise hem EUCAST disk difüzyon yöntemi hem Vitek 2 Compact antibiyotik duyarlılık kartı AST-GN325 ile çalışıldı.
HADT GSBL tarama önerisi (sefotaksim, 5 μg – seftazidim, 10 μg diskleri) ve HADT yöntemiyle yapılan kombine disk testi[3] (sefotaksim +/- klavulonik asit ve seftazidim +/- klavulonik asit) değerlendirildi (Şekil 1). HADT kombine disk testi, EUCAST tarafından önerilen bir yöntem olmayıp, çalışmamızda 24 saat sonra değerlendirilen klasik EUCAST kombine disk testi HADT olarak uygulandı. Değerlendirme kriteri olarak EUCAST kombine disk testinin kriterleri kullanıldı. GSBL üretimi aynı zamanda EUCAST disk difüzyon tarama kriterleri, kombine disk yöntemi ve Vitek 2 Compact otomatize sistemi uzman kurallarına göre değerlendirildi.
Karbapenemaz üretiminin tespiti için HADT tarama önerisi (meropenem, 10 μg disk) değerlendirildi. Aynı zamanda karbapenemaz üretimi, EUCAST disk difüzyon tarama kriterleri (meropenem, 10 μg disk) ve Vitek 2 Compact otomatize sistemi uzman kurallarına göre değerlendirildi.
HADT ile elde edilen sonuçlar, EUCAST disk difüzyon yöntemi ve otomatize sistem sonuçlarıyla karşılaştırıldı. HADT ile test sonuçlanma süreleri değerlendirildi. HADT yönteminin konvansiyonel yöntemlerle kategorik uyumu ve çok büyük hata oranları belirlendi.
BULGULAR
Çalışma kapsamında toplam 90 izolat değerlendirilmiştir. EUCAST tarafından sınır değer tabloları yayımlanmış olan bakteriler yönünden elde edilen toplam 74 (%82.2) izolatın, 31’i Klebsiella pneumoniae, 35’i Escherichia coli, dördü Acinetobacter baumannii ve dördü Pseudomonas aeruginosa olmak üzere, EUCAST HADT yöntemiyle antimikrobiyal duyarlılıkları belirlenmiştir. EUCAST HADT yönteminin henüz kapsamadığı 14 (%15.6) izolatın 12’si diğer Enterobacterales üyesi (dört Enterobacter cloacae, üç Serratia marcescens, iki Enterobacter aerogenes, iki Proteus mirabilis, bir Morganella morganii) ve ikisi diğer non-fermentatif bakteri (bir Burkholderia cepacia, bir Stenotrophomonas maltophilia) olarak saptanmıştır. Sadece bir hastanın kan kültürü şişesinden yapılan Gram boyamada aynı morfolojik özellikteki gram-negatif bakteriler HADT yöntemiyle test edilen antibiyotiklerin tümüne duyarlıydı ancak kan kültürü şişesinden yapılan konvansiyonel ekimlerde aynı antibiyotik duyarlılık sonucuna sahip iki farklı bakteri tespit edilmiştir (2/90; %2.2). P.aeruginosa ve E.coli şeklinde tanımlanan izolatlar çalışma kapsamı dışında tutulmuştur.
EUCAST HADT sınır değer tablolarına göre değerlendirilen izolatların (n= 74) test sonuçlanma süreleri Grafik 1’de gösterilmiştir.
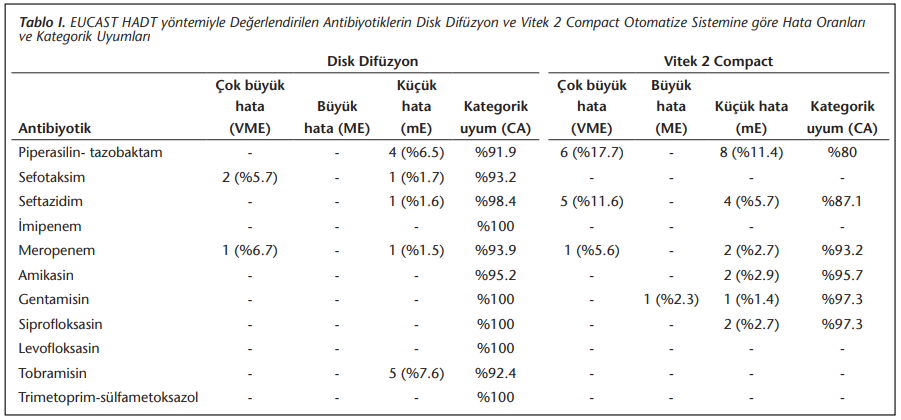
HADT yöntemi için ortalama kategorik uyum. otomatize sistemle %91.8; disk difüzyon yöntemiyle %96.8 bulunmuştur. HADT yönteminde otomatize sistemle karşılaştırıldığında piperasilin-tazobaktam (%17.7), seftazidim (%11.6) ve meropenemde (%5.6); disk difüzyon yöntemiyle karşılaştırıldığında ise sefotaksim (%5.7) ve meropenemde (%6.7) çok büyük hata tespit edilmiştir (Tablo 1).
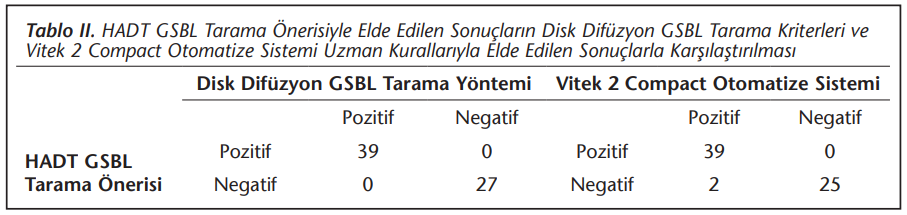
HADT tarama önerisine göre 39 izolatta GSBL varlığı düşünülmüştür. Disk difüzyon GSBL tarama kriterleriyle yapılan değerlendirme, HADT GSBL tarama önerisi sonuçlarıyla %100 uyumlu bulunmuştur (Tablo 2).
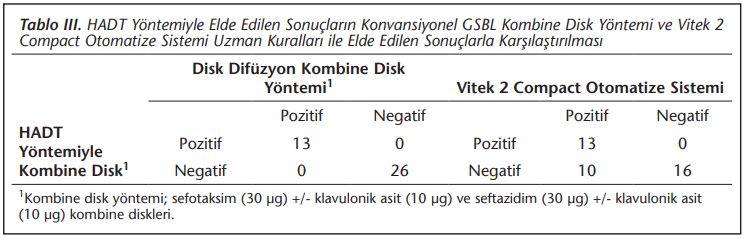
Kombine disk yöntemiyle 13 izolatta (13/39; %33.3) GSBL varlığı doğrulanmıştır. Konvansiyonel disk difüzyon yöntemi ve HADT yöntemiyle yapılan kombine disk testlerinin sonuçları %100 uyumlu bulunmuştur (Tablo 3).
Otomatize sistemin uzman kurallarla yaptığı değerlendirme dikkate alındığında, HADT GSBL tarama kriterleriyle negatif saptanan iki (2/66; %3) ve HADT GSBL kombine disk yöntemiyle negatif saptanan 10 (10/39; %25.6) izolatta otomatize sistem GSBL varlığı yönünde uyarı vermiştir.
Karbapenemaz üretiminin tespiti için HADT tarama önerisi, disk difüzyon tarama önerisi ve otomatize sistem sonuçları karşılaştırıldığında, yöntemler karbapenemaz varlığını taramada %100 uyumlu saptanmıştır (Tablo 4).
TARTIŞMA
Çalışmamızda pozitif alarm veren kan kültürü şişelerinden yapılan Gram boyama ile aynı morfolojide gram-negatif bakteri saptananlarda hızlı disk difüzyon yöntemi EUCAST HADT’nin kullanımının değerlendirilmesi amaçlanmıştır. HADT yöntemi, sepsis olgularında antibiyotik duyarlılık profilinin aynı gün içinde tespit edilmesini sağlayarak uygun antimikrobiyal tedaviye başlamada klinisyene yol gösterici olarak kullanılabilir ve hasta sağkalım oranlarını arttırabilir.
Çalışmamızda sepsis olgularında en sık sırasıyla, E.coli (n= 35; %39) ve K.pneumoniae (n= 31; %34) izolatları saptanmıştır.
Périllaud ve arkadaşlarının yaptığı çalışmada[4] pozitif kan kültürü şişesinden izole edilen 110 Enterobacterales üyesi arasında en sık tespit edilen izolatlar çalışmamıza benzer şekilde E.coli (n= 68; %62) ve K.pneumoniae (n= 18; %6)’ izolatlarıdır. Diğer Enterobacterales üyeleri olarak Enterobacter cloacae (n= 10; %9), Enterobacter aerogenes (n= 3; %3), Klebsiella oxytoca (n= 3; %3), Proteus mirabilis (n= 2; %2), Citrobacter freundii (n= 2; %2), Serratia marcescens (n= 2; %2), Citrobacter koseri (n= 1; %1) ve Salmonella enterica (n= 1; %1) tespit edilmiştir. Çalışmada Enterobacterales üyeleri için HADT yönteminin EUCAST disk difüzyon yöntemiyle kategorik uyumu %97.7; küçük hata %1.4, büyük hata %0.4 ve çok büyük hata oranı %0.5 olarak bulunmuştur. Test ettikleri antibiyotikler arasında %100 uyum saptadıkları antibiyotikler ise imipenem ve gentamisindir. Sefotaksim, trimetoprim-sülfametoksazol ve amikasin için %98’den fazla kategorik uyum gözlenmiştir.
Çalışmamızda benzer şekilde imipenem, gentamisin, siprofloksasin, levofloksasin ve trimetoprim-sülfametoksazol antibiyotikleri için HADT ile disk diffuzyon yöntemi arasında %100 kategorik uyum elde edilmiştir. Çalışmamızda HADT yöntemiyle otomatize sistem arasındaki kategorik uyum %91.8; disk difüzyon yöntemiyle %96.8’dir.
Martins ve arkadaşlarının yaptığı çalışmada[5] Enterobacterales üyeleri için HADT yönteminin EUCAST disk difüzyon yöntemiyle kategorik uyumu %94.4; küçük hata %4.3, büyük hata %0.6 ve çok büyük hata oranı %0.4 olarak bulunmuştur. Piperasilin-tazobaktam en yüksek küçük hata (%35) ve büyük hata (%5) gösterirken en yüksek çok büyük hata gentamisin ve tobramisin ile gözlenmiştir. HADT sınır değerlerine dayanan en iyi kategorik uyumu gentamisin (%98.4) ve siprofloksasin (%94.6) göstermiştir.
Çalışmamızda en yüksek çok büyük hata, otomatize sistemle karşılaştırıldığında piperasilin-tazobaktam, seftazidim ve meropenem ile; disk difüzyon yöntemiyle karşılaştırıldığında ise sefotaksim ve meropenem ile saptanmıştır.
Jasuja ve arkadaşlarının yaptığı çalışmada[6], 894 kan kültürü şişesi değerlendirilmiş, HADT yöntemi ile Vitek 2 otomatize sistemi arasındaki kategorik uyum %97 olarak bulunmuştur. Çok büyük hata ve büyük hata piperasillin-tazobaktam ve siprofloksasin antibiyotiklerinde tespit edilmiştir. Antibiyogram raporlama süreleri HADT ve otomatize sistem ile sırasıyla minimum 6:57 saat ve 24:39 saat bulunmuştur. Rapor verme süresinde kısalma, ortalama 17:30 saat olarak tespit edilmiştir.
Çalışmamızda elde ettiğimiz HADT’nin sonuçlanma süreleri; E.coli izolatları için en sık sekizinci saat (n= 18; %24) ve K.pneumoniae izolatları için altıncı saat (n= 16; %22) olarak tespit edilmiştir. P.aeruginosa ve A.baumannii izolatlarında HADT’nin sonuçlanma süreleri ise sırasıyla altıncı ve sekizinci saat olarak belirlenmiştir. Diğer çalışmalardan elde edilen sonuçlara benzer şekilde, dördüncü saatte antimikrobiyal duyarlılık testlerini sonuçlandırdığımız E.coli ve K.pneumoniae izolatları olmakla birlikte bu sayı altıncı ve sekizinci saatlere göre daha düşüktür. P.aeruginosa ve A.baumannii izolatlarında ise dördüncü saatte sonuç elde edilememiştir.
Soo ve arkadaşlarının yaptığı çalışmada[7], 194 kan kültürü şişesinde gram-negatif basil üremesi olan izolatlar değerlendirilmiş; HADT yöntemiyle otomatize sistemin sonuçları karşılaştırıldığında en yüksek büyük hata oranları E.coli (5/9; %55.6) ve P.aeruginosa (1/1; %100) için piperasilin-tazobaktamda saptanmıştır. Enterobacterales üyelerinde karbapenemaz üretiminin fenotipik tespiti için sekizinci saatte okunan zon çapının 17 mm tarama sınır değeri olarak alınabileceği; alternatif olarak, ertapenem veya temosilin disklerinin dahil edilmesinin, OXA-48 gibi zayıf hidrolitik aktivite gösteren karbapenemazların saptanma duyarlılığını artırabileceği düşününülmüştür.
Fröding ve arkadaşlarının yaptığı çalışmada[8], GSBL ve karbapenemaz üretiminin HADT ile fenotipik tespiti için Confirmkit 98011 ROSCO Diagnostica A/S (Taastrup, Danimarka) ve Mast Group Ltd.’den (Bootle, İngiltere) tablet kitleriyle hızlı bir şekilde okuma değerlendirilmiştir. Klavulanat ile kombine fenotipik testler kullanıldığında AmpC beta-laktamazların varlığı GSBL varlığını maskeleyebilmektedir. Sefoksitine dirençli izolatlar bu nedenle sonuçsuz olarak sınıflandırılmış; bu izolatların ek testlerle daha fazla araştırılması gerektiği belirtilmiştir. Çalışmamızda dokuz K.pneumoniae izolatı HADT tarama kriterlerine göre GSBL pozitif saptanmış; aynı izolatlar HADT çift disk sinerji testine göre negatif bulunmuş; bunun AmpC beta-laktamaz varlığına bağlı olabileceği düşünülmüştür.
Hombach ve arkadaşlarının yaptığı çalışmada[9], meropenem diskinin, Enterobacterales üyelerindeki KPC, NDM, VIM veya OXA-48 pozitifleri ve A, B ve D sınıfı karbapenemazı olanları etkili bir şekilde tespit ettiği; temosilin diskinin ise, 6-8. saatte OXA-48 pozitif izolatları tamamen ayırt ettiği gösterilmiştir. Çalışmamızda HADT meropenem tarama kriteri kullanılarak elde edilen sonuçlar, disk difüzyon ve otomatize sistemle elde edilen sonuçlarla tam uyumlu bulunmuştur.
Jasuja ve arkadaşlarının çalışmasında[6], sırasıyla tüm pozitif kan kültürü şişeleri için subkültürler ve Gram boyama işlemleri yapılmış; servislere pozitif kan kültürü bilgisi ve Gram boyama sonuçları telefon ve elektronik raporlamayla bildirilmiş; monobakteriyal kan kültürü şişeleri HADT için işleme alınmıştır. Ön rapor olarak altı saatlik üreme sonrası MALDI-TOF MS kullanılarak yapılan bakteri tanımlaması ve HADT sonuçları bildirilmiş, ek rapor olarak Vitek 2 panelleri kullanılarak yapılan duyarlılık sonuçları ertesi gün raporlanmıştır. Çalışmamız, benzer şekilde bir laboratuvar raporlama akışının uygulanabileceğini göstermiştir. Sonuç olarak çalışmamız, EUCAST HADT yöntemi ve sınır değer tabloları kullanılarak özellikle altıncı saatteki okumanın kan kültürlerinde antimikrobiyal duyarlılık sonuçlarını önceden tahmin etmek için tıbbi mikrobiyoloji laboratuvarlarında kullanılabileceğini göstermektedir. EUCAST HADT yönteminin rutin laboratuvarlarda uygulanabilir olduğunu ve düşük test maliyetiyle hızlı sonuç vermede kullanılabileceğini ancak çok büyük hataların olması, sonuçların standart yöntemlerle de doğrulanması gerektiğini göstermiştir.
ETİK KURUL ONAYI
Bu çalışma, Nisan 2019-Kasım 2019 tarihleri arasında prospektif olarak gerçekleştirilmesi nedeniyle etik kurul onayı gerekmemektedir.
ÇIKAR ÇATIŞMASI
Yazarlar bu makale ile ilgili herhangi bir çıkar çatışması bildirmemişlerdir.
KAYNAKLAR
- European Committee on Antimicrobial Susceptibility Testing (EUCAST). EUCAST Zone diameter breakpoints for rapid antimicrobial susceptibility testing (RAST) directly from blood culture bottles version 1.1. EUCAST; 02/05/2019 [updated 26/06/2020]. Available from: https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/RAST/EUCAST_RAST_Breakpoint_Table_v_1.1_final_PDF.pdf
- EUCAST. Screening for ESBL and carbapenemases in E.coli and K.pneumoniae for epidemiological purposes as part of the RASTprocedure version 1.0. 02/05/2019 [updated 26/06/2020]. Available from: https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/RAST/RAST_detection_of_resistance_mechanisms_Final.pdf
- EUCAST. EUCAST guidelines for detection of resistance mechanisms and specific resistances of clinical and/or epidemiological importance version 2.0 11/07/2017 [updated 26/06/2020]. Available from: https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/Resistance_mechanisms/EUCAST_detection_of_resistance_mechanisms_170711.pdf
- Périllaud C, Pilmis B, Diep J, Péan de Ponfilly G, Vidal B, Couzigou C, et al. Prospective evaluation of rapid antimicrobial susceptibility testing by disk diffusion on Mueller-Hinton rapid-SIR directly on blood cultures. Diagn Microbiol Infect Dis 2019; 93(1): 14-21.
- Martins AS, Wink PL, Pereira DC, Souza AC, Aquino VR, Barth AL. Rapid antimicrobial susceptibility of Enterobacteriaceae by disk diffusion directly from blood culture bottles using the EUCAST RAST breakpoints. J Glob Antimicrob Resist 2020; 22: 637-42.
- Jasuja JK, Zimmermann S, Burckhardt I. Evaluation of EUCAST rapid antimicrobial susceptibility testing (RAST) for positive blood cultures in clinical practice using a total lab automation. Eur J Clin Microbiol Infect Dis 2020; 39(7): 1305-13.
- Soo YT, Waled SNMB, Ng S, Peh YH, Chew KL. Evaluation of EUCAST rapid antimicrobial susceptibility testing (RAST) directly from blood culture bottles. Eur J Clin Microbiol Infect Dis 2020; 39(5): 993-8.
- Fröding I, Vondracek M, Giske CG. Rapid EUCAST disc diffusion testing of MDR Escherichia coli and Klebsiella pneumoniae: inhibition zones for extended-spectrum cephalosporins can be reliably read after 6 h of incubation. J Antimicrob Chemother 2017; 72(4): 1094-102.
- Hombach M, Jetter M, Keller PM, Blöchliger N, Kolesnik-Goldmann N, Böttger EC. Rapid detection of ESBL, carbapenemases, MRSA and other important resistance phenotypes within 6-8 h by automated disc diffusion antibiotic susceptibility testing. J Antimicrob Chemother 2017; 72(11): 3063-9.
İletişim (Correspondence):
Dr. Gizem Erdoğan,
Ankara Eğitim ve Araştırma Hastanesi,
Tıbbi Mikrobiyoloji Kliniği.
E-posta (E-mail):gizemonurel@hotmail.com