HBsAg N�tralizasyon Testinin Hepatit B Hastalığının
Tanı Algoritmasındaki Yeri ve �nemi
The Significance and Place of HBsAg Neutralization Test in the
Diagnosis and Algorithm of Hepatitis B Infection
�zlem AYTA�1, Alparslan TOYRAN1, Altan AKSOY1
1 Ankara Numune Eğitim ve Araştırma Hastanesi, Tıbbi Mikrobiyoloji Laboratuvarı, Ankara.
1 Ankara Numune Training and Research Hospital, Medical Microbiology Laboratory, Ankara, Turkey.
�Z
Hepatit B virusu (HBV) enfeksiyonunun tanısı serolojik, virolojik, biyokimyasal ve karaciğerin histolojik g�stergeleri ile değerlendirilmektedir. Bu �alışmanın amacı, HBsAg n�tralizasyon testinin hepatit B enfeksiyonu tanı algoritmasındaki yeri ve �nemini araştırmaktır. Ankara Numune Eğitim ve Araştırma Hastanesi Tıbbi Mikrobiyoloji Laboratuvarına Eyl�l 2014-Mayıs 2016 tarihleri arasında HBsAg testi i�in gelen ven�z kan �rneklerinden her bir hasta i�in reaktif olduğu kabul edilen (≥ 0.9 S\CO) ve sınır değer olarak kabul ettiğimiz (0.9 ≤ S\CO ≤ 30) serum �rnekleri iki kez �alışılmıştır. İki �alışmada da reaktif olan toplam 105 hastaya ait �rnek �alışmaya dahil edilmiştir. Bu �rnekler laboratuvarımızda rutin olarak uygulanan n�tralizasyon konfirmasyon testi ile değerlendirildikten sonra, �rnekler uygun koşullarda saklanarak HBV DNA i�in ger�ek zamanlı PCR testi ve HBeAg, anti-HBeAg, anti-HBc IgM, anti-HBc total antikor testleri ELISA ile �alışılmıştır. HBsAg tespit edilen 105 �rnek n�tralizasyon testi ile �alışılmıştır. HBsAg varlığı 105 �rnekten 67 (%63.8)'sinde n�tralizasyon testi ile doğrulanmış ve n�tralizasyon testi pozitif 67 hastadan HBV DNA'sı ve anti-HBc total antikor testi negatif olan 2 (%2.3) (yalancı pozitif n�tralizasyon testi) hasta tespit edilmiştir. �alışmaya dahil edilen 105 �rnekten 78 (%74.3)'inde anti-HBc total antikor testi pozitif tespit edilmiştir. Ancak anti-HBc total antikor testi pozitif 78 hastadan n�tralizasyon testi ve HBV DNA'sı negatif olan 13 (%16.7) (yalancı pozitif anti-HBc total testi) hasta bulunmuştur. HBsAg değeri 5 S/CO'dan k���k veya eşit olan �rneklerde HBV DNA pozitifliğinin HBsAg 5 S/CO'dan b�y�k olan �rneklere g�re daha az oranda olduğu istatistiksel olarak anlamlı tespit edilmiştir (p= 0.020). �alışmamızda kullanılan n�tralizasyon testinin birim fiyatı 17,00 TL iken, HBV DNA'nın birim fiyatının 55,00 TL olduğu saptanmıştır. Hasta bazında n�tralizasyon testi HBV DNA testi yerine tercih edildiğinde 38,00 TL gibi bir kazan� sağlanmaktadır. HBsAg titresi 5 S/CO'dan k���k ya da eşit iken doğrulama testi olarak n�tralizasyon testinin kullanılması, HBV DNA �alışılmasına gerek kalmadan test maliyetini olduk�a d�ş�receği saptanmıştır. HBsAg değeri 5 S/CO'dan b�y�k olan �rneklerde n�tralizasyon testi negatif bulunduğunda anti-HBc total antikor sonucu da negatif tespit edilirse HBV DNA'ya ihtiya� duymadan sonu� verilebileceği d�ş�n�lm�şt�r. Ancak n�tralizasyon testi negatif iken anti-HBc total antikor testi pozitif tespit edilirse, anti-HBc total antikor ve n�tralizasyon test sonu�larındaki uyumsuzluğu ortadan kaldırmak i�in HBV DNA �alışılması gerekmektedir. �alışmamızda aynı zamanda, anti-HBc total antikor testinin yalancı pozitifliğini (%16.7) y�ksek tespit ettiğimiz i�in tarama testi olarak HBsAg ile birlikte anti-HBc total antikor testinin kullanılmasının bir �st�nl�k getirmediği tespit edilmiştir.
Anahtar s�zc�kler: HBsAg; HBsAg n�tralizasyon testi; anti-HBc total.
ABSTRACT
The diagnosis of hepatitis B virus infection is evaluated serologically, virologically, biochemically, and with histologic liver indicators. The aim of this study was to investigate the place and significance of the HBsAg neutralization test in the diagnostic algorithm for hepatitis Binfection. From the venous blood samples sent to Ankara Numune Education and Research Hospital Medical Microbiology Laboratory between September 2014 and May 2016 for HBsAg test, serum samples regarded each patient as reactive (≥ 0.9 S\CO) , 9 ≤ S ≤ CO ≤ 30) were studied twice. A total of 105 samples which were reactive in both analyses were included in the study. After the evaluation of these samples by neutralization confirmation test, which is routinely performed in our laboratory, the samples were stored under optimal conditions and studied for HBV DNA with the real-time PCR and for HBeAg, anti-HBeAg, anti-HBc IgM, and anti-HBc total antibody assays by ELISA. The 105 samples, in which HBsAg was detected, were analyzed with the neutralization test. The presence of HBsAg was confirmed by neutralization test in 67 of 105 samples (63.8%), and of these patients, two patients (2.3%) had negative HBV DNA and anti-HBc total antibody test (false positive neutralization test). Of the 105 samples included in the study, the anti-HBc total antibody test was positive in 78 patients (74.3%). However, out of these 78 patients who were positive for the anti-HBc total antibody test, there were 13 patients (16.7%) with negative neutralization and HBV DNA test results (false positive anti-HBc total antibody test). The HBV DNA positivity was detected significantly lower in samples with HBsAg level ≤ 5 S/CO compared to the samples with HBsAg level > 5 S/CO (p= 0.020). Also, if the unit price of the neutralization test used in our study was considered, the cost was 17,00 TL while the unit price of HBV DNA test was 55,00 TL. Utilization of the neutralization test instead of HBV DNA test provides a saving of 38,00 TL per patient. The use of the neutralization test as a validation test when the HBsAg titre was less than or equal to 5S/CO will significantly reduce the cost of the test without the need for HBV DNA test. We suggest that if both the neutralization test and the anti-HBc total antibody test is negative in a sample with an HBsAg titration higher than 5 S/CO, the decision can be made without the need for HBV DNA test. However; if the neutralization test is negative, but the anti-HBc total antibody test is positive, then HBV DNA needs to be determined to eliminate the inconsistency between neutralization and anti-HBc total antibody assays. At the same time, we found that the use of anti-HBc total antibody test along with HBsAg as a screening test did not provide any advantage since the anti-HBc total antibody test was detected to have a high false positivity (16.7%) rate.
Keywords: HBsAg; HBsAg neutralization test; anti-HBc total.
Geliş Tarihi (Received): 06.01.2017 • Kabul Ediliş Tarihi (Accepted): 08.03.2017
GİRİŞ
Hepatit B virusu (HBV), Hepadnaviridae ailesi �yesi, k���k bir DNA virusudur1. HBV, kanda y�ksek konsantrasyonda bulunmakta; ayrıca semen, vajinal salgılar ve diğer v�cut sıvılarında da bulunabilmektedir. HBV enfeksiyonu kendini sınırlayabildiği gibi kronikleşebilmektedir. Kronik enfeksiyon riski virusun insanlara bulaştığı yaş ile ilgilidir ve k���k �ocuklarda y�ksek seviyede g�r�lmektedir. Enfekte bebeklerin yaklaşık %90'ında ve 1-5 yaş arası �ocukların %25-50'sinde enfeksiyon kronikleşmektedir. Erişkinlerin ise %95'i tamamen� iyileşmekte ve kronikleşme olmamaktadır2.
D�nya Sağlık �rg�t� (DS�) 2016 verilerine g�re; d�nya genelinde ortalama 240 milyon insan kronik hepatit B hastasıyken, her yıl 686.000'den fazla kişi siroz ve� karaciğer kanseri de dahil olmak �zere� hepatit B'nin komplikasyonlarından dolayı hayatını kaybetmektir3.
Hepatit B taşıyıcıların prevalansı d�nya �zerinde d�ş�k (< %2), orta (%2-7) ve y�ksek (≥ %8) olmak �zere �� grupta sınıflandırılmaktadır. T�rkiye %2-7 ile orta prevalans b�lgesinde yer almaktadır4,5.
T�rkiye'de 20 milyon kişinin HBV ile karşılaştığı ve 3.5-4 milyon taşıyıcının bulunduğu, 500.000-1.000.000 arasında kronik hepatit B'li hastanın var olduğu d�ş�n�lmektedir. T�rk Karaciğer Araştırmaları Derneği tarafından 2008-2011 yılları arasında �lkemizde ger�ekleştirilen TURK-HEP �alışmasında HBsAg (hepatit B y�zey antijeni) pozitifliği %4, hepatit B kor total antikoru (anti-HBc) pozitifliği %30.6, hepatit B surface y�zey antikoru (anti-HBs) pozitifliği ise %32 olarak saptanmıştır5. Karaciğer kanseri olgularının %60-80'i HBV ile ilişkilidir6. HBV enfeksiyonu, �lkemizde karaciğer hastalıklarının nedenlerinin başında gelmektedir. Bu virusa bağlı olarak gelişen akut hepatit, fulminan hepatit, kronik hepatit, karaciğer sirozu ve hepatosel�ler kanser (HSK) gibi hastalıklar, �lkemizin sağlık sorunları arasında �nemli yer tutmaktadırlar7,8.
HBV enfeksiyonunun tanısı serolojik, virolojik, biyokimyasal ve karaciğerin histolojik g�stergeleriyle değerlendirilmektedir9. Bu �alışmanın amacı HBsAg n�tralizasyon testinin hepatit B enfeksiyonunun tanı algoritmasındaki yeri ve �nemini araştırmaktır.
GERE� ve Y�NTEM
�alışmamıza Ankara Numune Eğitim ve Araştırma Hastanesi Mikrobiyoloji Laboratuvarına Eyl�l 2014-Mayıs 2016 tarihleri arasında HBsAg ELISA testi �alışılması i�in gelen ven�z kan �rneklerinden, yapılan ilk �alışmada kit prosed�rlerine g�re pozitif olan (≥ 0.9 S/CO)� fakat sınır değer olarak kabul ettiğimiz d�ş�k pozitif� (0.9-30 S\CO)�� HBsAg� tespit edilmiş,� aynı serum ile� yapılan ikinci �alışmada tekrar d�ş�k pozitif sonu� elde edilen 105 �rnek dahil edildi. �alışmaya dahil edilen �rneklerde n�tralizasyon testi �alışıldıktan sonra HBV DNA, HBeAg, anti-HBeAg, anti-HBc IgM ve anti-HBc total antikor �alışılmak �zere -80�C'de saklandı.
�alışmamızda HBsAg (DiaSorin, MurexHBsAgVersion 3, İtalya), HbeAg (DiaSorin, ETI-EBK PLUS, İtalya), anti-HBc IgM (DiaSorin, ETI-CORE-IGMK PLUS, İtalya) testleri ETI-Max 3000 cihazı kullanılarak �retici firmanın talimatları doğrultusunda ELISA testi yapılarak kalitatif olarak tespit edildi. Anti-HbeAg (DiaSorin, ETI-AB-EBK PLUS, İtalya), anti-HBc total antikor (DiaSorin, ETI-AB-COREK PLUS, İtalya) testleri ETI-Max 3000 cihazı kullanılarak �retici firmanın talimatları doğrultusunda� yarışmalı ELISA testi kullanılarak kalitatif olarak tespit edildi.
N�tralizasyon doğrulama testi i�in HBsAg'ye �zg� antikor ile (n�tralizasyon reaktifi)� n�tralizasyon prensibinden yararlanan Access HBsAg Confirmatory test (Beckman Coulter, ABD) kullanıldı. Sistem yazılımı tarafından otomatik olarak belirlenen hasta test sonu�ları kullanıldı. �rnek pozitifliğinin doğrulanması Access sistemi tarafından ger�ekleştirilen hesaplamalar 1.0 veya daha �zeri bir S\CO oranı ve %40 ya da �zeri bir inhibisyon y�zdesinin saptanmasına g�re kabul edildi.
HBV DNA izolasyonu QIAGEN-QIAsymhony cihazı ile Artus HBV QS-RGQ kitiyle kombinasyon halinde bulunan QIAsymphony DSP Virus/Pathogen Midi Kiti kullanılarak yapıldıktan sonra, HBV DNA'nın 134 bp'lik kor b�lgesini hedefleyen ArthusHBV QS- RGQ Kit (Qiagen, Almanya) ile ger�ek zamanlı PCR cihazında (ROTOR GENE Q, ORBETT ResearchPtyLtd, Avusturya) �retici firma �nerilerine uygun olarak HBV DNA kantitatif tespiti yapıldı.
İstatistiksel Analiz
Verilerin istatistiksel analizi SPSS for Windows 11.5 paket programında yapıldı. Değerlendirmede ki-kare testi kullanıldı. İstatistiksel anlamlılık sınırı p< 0.05 olarak kabul edildi.
BULGULAR
�alışmaya dahil ettiğimiz� 38 (%36.2)'i kadın, 67 (%63.8)'si ise erkek hastaya ait 105 �rneği ilk �alışmada elde ettiğimiz HBsAg testi S/CO değerlerine� g�re S/CO ≤ 5,� 5 < S/CO ≤ 10, 10 < S/CO < 20, ≥ 20 olmak �zere d�rt grupta incelenmiştir .
N�tralizasyon testi ile HBsAg'leri pozitif bulunan 105 �rnekten 67 (%63.8)'sinde HBsAg varlığı doğrulanmıştır. HBsAg pozitif tespit edilen �rneklerde HBsAg titresi arttık�a n�tralizasyon testinin pozitiflik oranındaki artış istatistiksel olarak anlamlı tespit edilmiştir (p= 0.001). �rneklerin hepsinin HBeAg ve anti-HBc IgM test sonu�ları negatif iken anti-HBe antikoru 73 (%69.5) �rnekte pozitif olarak tespit edilmiştir. �alışmaya dahil edilen 105 �rnekten 78 (%74.3)'inde anti-HBc total antikoru pozitif olarak tespit edilmiştir.
HBsAg'leri pozitif olarak tespit edilen �rneklerde HBsAg titresi arttık�a anti-HBc total antikor pozitifliğindeki artışın istatistiksel olarak anlamlı olduğu bulunmuştur (p= 0.024).
Ger�ek zamanlı PCR ile 105 �rneğin 23 (%21.9)'�nde HBV DNA pozitifliği tespit edilmiştir. HBV DNA'sı pozitif 23 hastadan 22'sinde HBV DNA'sının d�ş�k d�zeyde (< 1000 kopya/ml) pozitif olduğu saptanmıştır.
HBsAg değeri 5 S/CO'dan k���k veya eşit olan �rneklerde HBV DNA pozitifliğinin HBsAg 5 S/CO'dan b�y�k olan �rneklere g�re daha az oranda olduğu istatistiksel olarak anlamlı tespit edilmiştir (p= 0.020). HBV DNA sonucu negatif olarak saptanan 82 �rnekten 42 (%51.2)'sinin n�tralizasyon, anti-HBc total antikor ve anti-HBe antikor testleri pozitif olarak tespit edilmiştir.
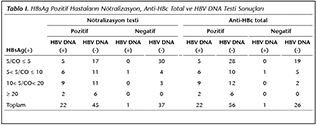
Anti-HBc total antikor ve n�tralizasyon testlerini birlikte değerlendirdiğimizde anti-HBc total antikor testi pozitif 78 hastadan 56 (%71.8)'sının HBV DNA'sı negatif tespit edilirken n�tralizasyon testi pozitif olan 67 hastadan 45 (%67.2)'inin HBV DNA'sı negatif olarak tespit edilmiştir. Anti-HBc total antikor testi pozitif olup DNA'sı negatif olan 56 hastadan 28 (%50)'inde HBsAg titresi 5 S/CO'dan k���k veya eşit olarak tespit edilmiştir (Tablo I).
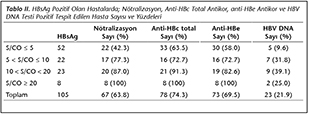
N�tralizasyon testi pozitif 67 hastadan, HBV DNA'sı ve anti-HBc total antikor testi negatif (yalancı� pozitif) olan 2 (%2.3) hasta saptanmıştır. Ancak anti-HBc total antikor testi pozitif 78 hastadan� n�tralizasyon testi ve HBV DNA'sı negatif olan 13 (%16.7) hasta tespit edilmiştir (yalancı pozitif anti-HBc total). Anti-HBc total antikor test sonucu yalancı pozitif olarak tespit edilen 13 hastanın 11 (%84.6)'inde ise HBsAg titresinin 5 S/CO'dan k���k veya eşit olduğu g�r�lm�şt�r. N�tralizasyon testinin ise HBsAg titresi 5 S/CO'dan k���k veya eşit iken yalancı pozitif sonu� vermediği saptanmıştır. �alışmamızda yalancı pozitif n�tralizasyon testi y�zdeleri hesaplanırken hastaların anti-HBc total antikor ve HBV DNA test sonu�larının birlikte negatif sonu� vermesi, yalancı pozitif anti-HBc total antikor testi y�zdeleri hesaplanırken ise n�tralizasyon testi ve HBV DNA test sonu�larının birlikte negatif� sonu� vermesi� esas alınmıştır (Tablo II).
N�tralizasyon testi negatif olup anti-HBc total antikor testi pozitif olan 14 �rnekten 13 (%92.8)'�nde HBV DNA negatif olarak tespit edilirken, 11 (%84.6)'inde HBsAg d�ş�k pozitif (5 S/CO'dan k���k veya eşit) olarak� tespit edilmiştir. Hem n�tralizasyon testi hem de anti-HBc total antikor testi negatif olan hastaların t�m�nde HBV DNA varlığı saptanmamıştır.
�alışmamızda kullanılan n�tralizasyon testinin birim fiyatı 17,00 TL iken HBV DNA testi birim fiyatının 55,00 TL olduğu belirlenmiştir. Hasta bazında n�tralizasyon testi HBV DNA testi yerine tercih edildiğinde 38,00 TL gibi bir kazan� sağlanmaktadır.
TARTIŞMA
Hepatit B enfeksiyonları, insanlığın en �nemli enfektif hastalıklarından biridir. Karaciğer kanseri ve siroz nedeniyle yılda yaklaşık 800.000 �l�me neden olduğu tahmin edilmektedir10.
HBV'ye ait antijenlerin veya antikorların hasta serumunda saptanmasını sağlayan serolojik testler, enfeksiyonun hangi evrede olduğunu belirlemede ve enfektivitenin değerlendirilmesinde yaygın olarak kullanılmaktadır11. Hepatit B enfeksiyonu tanı y�ntemleri gelişmiş ve gelişmekte olan �lkeler ile arasında ve hepatit B'nin d�ş�k ve y�ksek seviyede endemik olduğu �lkeler arasında farklılıklar� g�stermektedir. ABD gibi bazı gelişmiş �lkelerde devam eden hepatit B enfeksiyonu tanısı HBsAg ve n�tralizasyon testleriyle konulmaktadır. Hepatit B enfeksiyon oranının d�ş�k olduğu (< %3) gelişmiş �lkelerde b�yle bir uygulama m�mk�n olabilmektedir12,13.
2016 yılında yayınlanan ulusal kan ve kan bileşenleri rehberi HBsAg tarama testinde tekrarlayan reaktiflik saptanan numunelerin �rneklerin doğrulanması i�in HBsAg n�tralizasyon testi yapılması ya da tarama testinde reaktif HBsAg sonu�larının anti-HBc total testi ile değerlendirilmesini bu testin iki �alışmada reaktif tespit edilmesi durumunda sonucun pozitif olarak bildirilmesi ancak anti-HBc total antikor testinin reaksiyon vermemesi durumunda bu �rnekten tekrar n�tralizasyon testi �alışılarak sonucun doğrulanması gerektiğini �nermektedir14,15.
�alışmamızda HBsAg değeri 5 S/CO'dan k���k ya da eşit olup, n�tralizasyon testini negatif tespit ettiğimiz 30 (%57.7) hastadan 11 (%36.7)'inin anti-HBc total antikor testi pozitif bulundu. Bu hastaların HBV DNA'sı ise negatif olarak tespit edildi. HBsAg değeri 5 S/CO'dan k���k ya da eşit olduğunda n�tralizasyon testi pozitif bulunan 22 (%42.3) �rneğin tamamının anti-HBc total antikor testlerinin de pozitif olduğu g�r�ld�. �alışmamız verilerine dayanarak �zellikle HBsAg titresi 5 S/CO'dan k���k ya da eşit iken n�tralizasyon testinin anti-HBc total antikor ve HBV DNA testleri ile doğrulamaya gerek kalmadan tek başına HBsAg pozitifliğini doğrulamak i�in kullanılabileceğini d�ş�nmekteyiz.
Ancak �alışmamıza dahil ettiğimiz HBsAg'nin 5 S/CO'dan b�y�k olan �rneklerin n�tralizasyon, anti-HBc total antikor ve HBV DNA test sonu�larını incelediğimizde n�tralizasyon testi negatif 8 hastadan 5 (%62.5)'inin anti-HBc total antikor ve HBV DNA testleri negatif tespit edildi. Buna karşılık 8 hastadan 3 (%37.5)'�nde ise anti-HBc total antikor testi pozitif tespit edilmiş iken birinde HBV DNA'nın pozitif olduğu g�r�lm�şt�r. HBsAg değeri 5 S/CO'dan b�y�k olan �rneklerde n�tralizasyon testi negatif iken anti-HBc total antikor sonucu da negatif tespit edilirse HBV DNA'ya ihtiya� duymadan sonu� verilebileceği ancak n�tralizasyon testi negatif iken anti-HBc total antikor pozitif tespit edildiğinde anti-HBc total antikor ve n�tralizasyon test sonu�larındaki uyumsuzluğu ortadan kaldırmak i�in HBV DNA �alışılması gerektiğini d�ş�nmekteyiz.
"Centers for Disease Control and Prevention (CDC)", HBsAg pozitif test sonu�larının ger�ek pozitif olma ihtimalini değerlendirmek i�in HBV enfeksiyonunun diğer serolojik belirte�lerinin (anti-HBc total antikor, anti-HBc IgM, HBV DNA gibi) kullanılabileceğini ancak pozitif bulunan HBsAg test sonu�larının bir doğrulama testi ile (�rn. n�tralizasyon testi) kontrol edilmesini �nermektedir16. O'Brien ve arkadaşlarının17 yaptığı �alışmada yalnızca zayıf pozitif (S/CO < 5) HBsAg EIA test sonu�larının n�tralizasyon testi ile daha ayrıntılı değerlendirilmesi �nerilmektedir. Bizim �alışmamızda da HBsAg sonucu 5 S/CO'dan k���k ya da eşit olan 52 �rnekten 30 (%57.7)'unun doğrulama testi negatif bulunurken, bu hastaların HBV DNA sonu�larına baktığımızda hepsinin HBV DNA'sının negatif sonu� verdiği g�r�lmektedir (yalancı pozitif HBsAg). �alışmamızda HBsAg 5 S/CO'dan k���k ya da eşit olduğunda n�tralizasyon testinin doğrulama oranını %42.3, S/CO oranı 5< S/CO ≤ 10, 10 < S/CO < 20 ve ≥ 20 olduğunda sırasıyla n�tralizasyon testinin doğrulama oranlarının %77.3, %87.0, %100.0 olduğu bulunmuştur. �zellikle S/CO oranı 5'ten k���k olan �rneklerde n�tralizasyon testi yapılarak yalancı pozitif HBsAg sonu�larının saptanarak, hastalarda yanlış pozitif sonu�lara bağlı oluşacak anksiyetenin �n�ne ge�ileceği, test karmaşasını ortadan kaldırarak sonu� verme s�resini kısaltırken aynı zamanda gereksiz HBV DNA �alışılmasını engelleyeceği ve maliyeti azaltacağı d�ş�ncesindeyiz. Ayrıca �alışmamızda kullanılan n�tralizasyon testinin birim fiyatı 17,00 TL iken, HBV DNA'nın birim fiyatı 55,00 TL olarak saptanmıştır. Hasta bazında n�tralizasyon testinin HBV DNA testi yerine tercih edilmesi durumunda 38,00 TL kar sağlanmaktadır.
Shao ve arkadaşlarının18 2012 yılında yapmış olduğu bir �alışmada, 144 �rnekte başlangı� eşik değeri 0.9-10 olan 85 (%59.0) �rneğin doğrulama testleri sonucu pozitif, başlangı� eşik değeri 1.0-4.0 arasında olan 59 (%41.0) �rneğin doğrulama testleri sonucu ise negatif olarak tespit edilmiştir. �alışmalarında ilk test sonu�larının eşik değer indeksi arttık�a doğrulama testinin pozitiflik oranının da arttığını, başlangı� eşik değeri birden k���k veya eşitken doğrulama testinin oranı 0 iken, 4'ten b�y�k ya da eşitken doğrulama oranını %100 olarak tespit etmişlerdir.
Wan-Zhou ve arkadaşlarının19 2013 yılında yapmış oldukları �alışmada yanlış pozitif olarak elde edilen sonu�ları dışlamak i�in ilk testte pozitif sonu� veren �rneklerde konfirmasyon testinin gerekli olduğunu, �zellikle HBsAg testinin ilk reaktif sonu�ları 1.0 ≤ S/CO ≤ 9.0 olan �rneklerde konfirmasyon testi yapılması gerektiği �nerilmiştir. �alışmamızın sonu�larına g�re HBsAg'nin ilk reaktif sonucu 1.0 ≤ S/CO ≤ 5.0 olan �rneklerde n�tralizasyon testinin HBsAg pozitifliğini doğrulamak i�in kullanılabileceğini d�ş�nmekteyiz.
Chen ve Kaplan'ın 2006 yılında yaptıkları �alışmada20 zayıf pozitif 127 �rnekte viral y�k ve diğer serolojik HBV belirte�leri test edilmiştir. �alışmada yalancı pozitif sonu�ların gereksiz klinik takiplere, fazladan finansal giderlere neden olduğunu ve zayıf pozitif HBsAg sonucu veren �rneklerde n�tralizasyon testinin kullanılması �nerilmiştir. Chen ve Kaplan'ın yapmış olduğu bu �alışmada n�tralizasyon testi 127 �rnekten 38 (%29.9)'inde pozitif bulunurken, 89 (%70.1)'unda negatif elde edilmiştir. N�tralizasyon testi negatif olan bu 89 �rnekten 83 (%93.2)'�nde HBV DNA� tespit edilememiştir. Bu �rneklerin 6 (%6.8)'sında HBV DNA pozitif bulunmuş ve hepsinin viral y�k�n�n (9000 kopya/ml) d�ş�k olduğu tespit edilmiştir. N�tralizasyon sonucu pozitif olan 38 �rnekten 22 (%57.9)'sinde HBV DNA negatif iken 16 (%42.1) �rnekte HBV DNA pozitif olarak tespit edilmiştir. HBV DNA sonucu negatif olan 22 �rnekten altısında anti-HBs negatif/anti-HBc total antikor pozitif/anti-HBc IgM negatif tespit� edilmesi durumunda y�ksek ihtimalle ger�ek pozitif sonu� olduğu ancak HBV DNA'sının tespit edilebilecek d�zeyde olmadığı d�ş�n�lm�şt�r. �alışmamızda n�tralizasyon test sonucu pozitif olan 67 �rnekten 45 (%67.2)'inde HBV DNA testi sonucu negatif olarak tespit edildi. Bu hastalardan 42 (%93.3)'sinin anti-HBe ve anti-HBc total antikor serolojik belirte�leri pozitif olarak bulundu ve bu �rneklerin y�ksek ihtimalle ger�ek pozitif olduğu ancak tespit edilebilecek d�zeyde HBV DNA i�ermedikleri d�ş�n�lm�şt�r.
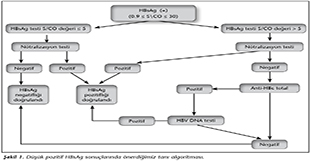
Sonu� olarak �alışmamızda elde edilen verilere g�re� �zellikle HBsAg titresi 5 S/CO'dan k���k ya da eşit iken n�tralizasyon testinin anti-HBc total antikor ve HBV DNA testleriyle doğrulamaya gerek kalmadan tek başına HBsAg pozitifliğini doğrulamak i�in kullanılabileceği g�sterilmiştir. Bu ama�la bir tanı algoritması geliştirilmiştir (Şekil 1). Bu durum yalancı pozitifliklere bağlı hastalarda oluşacak endişenin �n�ne ge�erken, aynı zamanda test karmaşasını engelleyerek maliyetinde d�şmesini sağlayacaktır. Kanada gibi bazı �lkelerde hepatit B tarama testi olarak HBsAg ile birlikte anti-HBc total antikor testi birlikte değerlendirilmektedir. �lkemiz gibi orta endemisite b�lgesinde olan �lkelerde anti-HBc total antikor testinin yalancı pozitiflik oranı y�ksek seviyede saptanmaktadır. �alışmamızda anti-HBc total antikor testinin yalancı pozitifliği y�ksek tespit edildiğinden tarama testi olarak HBsAg ile birlikte anti-HBc total antikor testinin kullanılmasının �st�nl�k getirmediği d�ş�n�lm�şt�r. T�m gruplara baktığımızda n�tralizasyon testinin yalancı pozitifliği %2.3 iken, anti-HBc total antikor testinin yalancı pozitiflik oranı %16.7 olarak tespit edilmiştir. Bu durumda HBsAg reaktifliğini doğrulamak i�in �ncelikli olarak anti-HBc total antikor testi yerine n�tralizasyon testinin kullanılması daha doğru sonu�lar elde edilmesini sağlayacaktır. �alışmamızda aynı zamanda 105 hastadan 73 (%69.5)'�nde anti-HBe testi pozitif olarak tespit edilmiş ve bu hastaların tamamında anti-HBc total antikor testi de pozitif olarak saptanmıştır. Hepatit B taramasında HBsAg testi ve anti-HBe testinin birlikte değerlendirilmesinin, HBsAg ve anti-HBc total antikor testinin birlikte değerlendirilmesine herhangi bir �st�nl�ğ� olmadığı d�ş�n�lm�şt�r.
KAYNAKLAR
- Hepadnaviridae. In: B�chen-Osmond C (ed), ICTVdB The Universal Virus Database, version 3.� ICTVdB Management. 2003, Columbia University, New York. Erişim: http://www.ncbi.nlm.nih.gov/ICTVdb/ICTVdB/30000000.htm.
- Sağlık Bakanlığı T�rkiye Halk Sağlığı Kurumu. Bulaşıcı Hastalıkların Laboratuvar Tanısı i�in Saha Rehberi. Hepatit B ve D. Erişim: 28.09.2016. http://mikrobiyoloji.thsk.saglik.gov.tr/ums/H/Hepatit-B-ve-D.pdf.
- World Health Organization. Hepatitis B. Erişim: 21.09.2016. http://www.who.int/mediacentre/factsheets/fs204/en/.
- Koziel MJ, Siddiqui A. Hepatitis B virus and hepatitis D virus, pp: 1864-90, In: Mandell GL, Bennett JE, Dolin R (eds), Principles and Practice of Infectious Diseases, 2005, 6th ed. Churchill Livingstone, New York.
- Tozun N, �zdogan OC, Cakaloglu Y, et al. A nation wide prevalence study and risk factors for hepatitis A, B, C and D infections in Turkey. Hepatology 2010; 52(Supp 1): 697A.
- Lai CL. Discovery and classification, pp: 1-8, In: Lai CL, Locarnini S (eds), Hepatitis B virus, 2002. International Medical Press, London.
- Değertekin H. Viral hepatitlerin d�nyada ve �lkemizdeki epidemiyolojisi. Aktuel Tıp Dergisi 1997; 2: 119-22.
- Mıstık R, Balık İ. T�rkiye'de viral hepatitlerin epidemiyolojik analizi, pp: 10-55. In: Kılıcturgay K, Badur S (eds), Viral Hepatit 2001. İstanbul, Viral Hepatitle Savaşım Derneği.
- Dienstag JL. Hepatitis B virus infection. N Engl J Med 2008; 359(14): 1486-500.
- Lavanchy D, Kane M. Global epidemiology of hepatitis B virus infection, pp: 187-203, Global Epidemiology of Hepatitis B Virus Infection, Part of the series, Molecular and Translational Medicine, 2016. Springer International Publishing, Switzerland.
- Robinson WS. Hepatitis B virus and hepatitis D virus, pp: 1652-84, In: Mandell GL, Bennett JE, Dolin R (eds), Principles and Practise of Infectious Diseases, 2000. Churchill Livingstone, New York.
- Chuang CH. Hepatitis B control program in Taiwan. Acta Paediatr Jpn 1989; 31(6): 645-8.
- Wong WC, Tsang KK. A mass hepatitis B vaccination programme in Taiwan: its preparation, results and reasons for uncompleted vaccinations. Vaccine 1994; 12(3): 229-34.
- Ertuğrul �r�� N, Yenicesu� İ. Ulusal Kan ve Kan Bileşenleri Hazırlama, Kullanım ve Kalite G�vencesi Rehberi, T�rkiye'de Kan Tedarik Sisteminin G��lendirilmesi Teknik Destek Projesi, 2016. TR0802.15-01/001.
- Centers for Disease Control and Prevention. Guidelines for Viral Hepatitis Surveillance and Case Management. Erişim: 25.09.2016 https://www.cdc.gov/hepatitis/statistics/surveillanceguidelines.htm.
- O'Brien JE. Hepatitis B surface antigen: decreased need for confirmation of reactive results. Clin Chem 2000; 46(4): 582.
- The GS HBsAg Confirmatory Assay 3,0 (BioRad), package insert 32594. Erişim: 26.09.2016. http://www.bio-rad.com/en-us/product/hepatitis-b/gs-hbsag-confirmatory-assay-3-0.
- Shao H, Li Y, Xu W, Zhou X. Increased need for testing to confirm initial weakly reactive results for hepatitis B virus surface antigen. Lab Med 2012; 43(4): 15-7.
- Wan-Zhou X, Yan L, Qing W, Ming W, Ze-gang W. Brief communication: comparison the diagnostic performance of four HBsAg ELISA kits. J Clin Lab Anal 2013; 27(4): 294-6.
- Chen D, Kaplan LA. Performance of a new-generation chemiluminescent assay for hepatitis B surface antigen. Clin Chem 2006; 52(8): 1592-8.
İletişim (Correspondence):
Uzm. Dr. �zlem Ayta�,
Elazığ Eğitim ve Araştırma Hastanesi,
Elazığ, T�rkiye.
Tel (Phone): +90 506 388 9345,
E-posta (E-mail): ozlemozlem5@hotmail.com