37 NANP ve 4 NVDP Epitoplu Plasmodium falciparum Rekombinant Circumsporozoite Proteinin Ekspresyonu ve Molek�ler Karakterizasyonu*
Production and Molecular Characterization of Plasmodium falciparum Recombinant Circumsporozoite Protein with 37 NANP and 4 NVDP Epitopes
Yunus UYAR1, Abd�ssamed AKŞİT2, Serkan KARACA2, Şirin Sahra CEYLAN2, Merve Y�R�K2
1 T�rk Kızılayı Kan Bağış Merkezi, Kayseri.
1 Turkish Red Crescent Blood Donation Center, Kayseri, Turkey.
2 Erciyes �niversitesi Tıp Fak�ltesi, Tıbbi Parazitoloji Anabilim Dalı, Kayseri.
2 Erciyes University Faculty of Medicine, Department of Medical Parasitology, Kayseri, Turkey.
* Bu �alışma Erciyes �niversitesi Bilimsel Araştırma Projeleri Birimi tarafından TDK-2014-5370 nolu proje ile desteklenmiş ve �alışmanın bir b�l�m� 18. Ulusal Parazitoloji Kongresi (29 Eyl�l-5 Ekim 2013, Denizli)'nde poster olarak sunulmuştur.
�Z
Plasmodium cinsine ait protozoan parazitlerin sebep olduğu sıtma, paraziter hastalıklar arasında en fazla �l�me neden olanıdır. Hastalık dişi Anofel sivrisineğin insanlardan kan emmesiyle bulaşmaktadır. D�nya Sağlık �rg�t� (DS�) verilerine g�re 2015 yılı i�erisinde 214 milyon yeni sıtma olgusu g�r�lm�ş ve buna bağlı olarak 438 bin �l�m olgusu ger�ekleşmiştir. Sıtmaya bağlı �l�mlerin %90'ı Afrika kıtasında g�r�lmektedir. Bu �l�mlerin %78'i beş yaş altı pop�lasyonu etkilemektedir. Sıtmaya karşı y�r�t�len yoğun m�cadele sonucunda 2000 ila 2015 yılları arasında hastalığın insidansı %37 azalmıştır. Hızlı ve etkin bir bi�imde tanı ve tedavisi ger�ekleştirildiğinde, sıtma iyileştirilebilir bir hastalıktır. Halihazırda sıtmaya karşı kullanılan ila�ların hemen hepsine karşı diren� gelişmiş durumdadır ve g�n�m�zde sıtmaya karşı tam etkili bir aşı ise hen�z geliştirilememiştir. 40 yıl �nce, radyasyon uygulanmış 1000 sivrisineğe maruz bırakılan kişilerde falciparum sıtmasına karşı steril immunite oluşturulmasıyla birlikte �alışmalar başlamıştır. Plasmodium'ların kompleks yapıları ve karmaşık hayat d�ng�leri ve �ok fazla antijenik yapılarının olması aşı �alışmalarını zorlaştırmaktadır. �zerinde en fazla �alışılan Circumsporozoite protein (CSP), g�n�m�zde lisans almaya en yakın aday olan RTS,S'in de yapısında bulunmaktadır. CSP, enfeksiyonun başlangıcı esnasında oynadığı �nemli rolden dolayı parazitin antijenik yapıları i�erisinde ilk tanımlananıdır. Plasmodium'ların major y�zey proteinidir. CSP ��z�nebilir bir proteindir ve Escherichiacoli h�creleri i�erisinde bu proteinin rekombinant formu �retilebilmektedir. NANP tekrar b�lgesi konak antikorları i�in hedef �zelliğindedir. G�n�m�zde sıtmaya karşı bir�ok protein ve DNA aşısı geliştirilmeye �alışılmaktadır. DS�'ye g�re �n�m�zdeki 20 yıllık d�nemde sıtma aşısının yapılabilmesi m�mk�nd�r. Bu �alışmada, P.falciparum CSP'nin rekombinant (rCSP) olarak �retilmesi ama�lanmıştır. �ncelikle CSP geni PCR ile �oğaltılmıştır. CSP geni pJET vekt�r�ne klonlanmış; daha sonra pET100 protein ekspresyon vekt�r�ne subklonlama yapılmıştır. Protein ekspresyonu i�in E.coli h�creleri kullanılmıştır. Bu işlemden sonra saflaştırma ve endotoksinlerden arındırma protokolleri uygulanmıştır. Sonu� olarak; P.falciparum genomik DNA'sından 1.182 bp'lik CSP geni elde edilmiştir. DNA dizi analizi ile gen klonlamasının doğruluğu ve CSP geninin DNA dizisi tespit edilmiştir. Elde edilen gen dizisi GenBank'a KT315396 kayıt no ile kaydedilmiştir. Plazmit i�erisine yerleştirilen CSP geni ile E.coli h�crelerinde rCSP eksprese edilmiştir. Western blot ile varlığı g�sterilen rCSP, saflaştırıldıktan sonra endotoksinlerinden arındırılmıştır. rCSP'nin aminoasit dizilimi ve 3 boyutlu şekli elde edilmiştir. CSP'nin rekombinant olarak �retilmesinin laboratuvarımızda ve �lkemizde yapılacak sıtma aşı �alışmalarına katkı sağlayacağı kanaatindeyiz.
Anahtar s�zc�kler: Sıtma; sıtma aşısı; Plasmodium falciparum; Circumsporozoite protein; bağışıklık.
ABSTRACT
Malaria is caused by the protozoan parasite Plasmodium, the leading cause of death amongst the parasitic diseases. The disease is transmitted to human by the bites of female Anopheles mosquitoes. According to the World Health Organization (WHO) data, there were an estimated 214 million malaria cases and estimated 438.000 deaths occurred worldwide, in 2015. It is observed that 90% of all the deaths due to malaria occur in Africa. 78% of these cases were children who are under five years old. Intensive malaria interventions helped to reduce malaria incidence by 37% between 2000 and 2015. Malaria is a curable disease if diagnosed and treated promptly and correctly. Drug resistance has developed against almost all anti-malarial drugs and an effective vaccine against malaria has not been developed yet. Vaccine studies initiated 40 years ago by sterile immunity against falciparum malaria through immunization by exposure to 1000 irradiated mosquitoes. Complex structures, complicated life cycles and various antigenic structures of Plasmodium species make vaccination studies difficult. Circumsporozoite protein (CSP), the most extensively studied protein is also present in the content of the vaccine candidate RTS,S which is currently closest to get license. CSP was the first described Plasmodium antigen because of its important role during initiation of the parasitic infection. CSP is the major surface coat protein of Plasmodium parasite. CSP is a soluble protein and recombinant form of the CSP can be produced in Escherichia coli. NANP repeat region is a target site for host antibodies. Recently many DNA, RNA and protein vaccine candidates are being developed against malaria. According to WHO, in the next 20 years period, malaria vaccine can be developed. In this study we aimed to produce recombinant CSP (rCSP). Initially, P.falciparum CSP gene was amplified by PCR. CSP gene was cloned in to the pJET cloning vector. The gene subcloned to the pET100 protein expression vector. E.coli cells were used for protein expression. After this process, purification and endotoxin removal protocols were performed. As a result, 1182 bp CSP gene was obtained from P.falciparum genomic DNA. Accuracy of cloning and DNA sequence of the CSP gene was determined with DNA sequence analysis. The gene sequence was recorded to the GenBank with a registration no KT315396. rCSP was expressed in E.coli cells. The existence of rCSP was verifiedwith Western Blot method and was purified and removed from endotoxins. rCSP aminoacid sequence and 3D shape was obtained.We believe that the production of recombinant CSP will enable us to contribute to the further malaria vaccine studies in our laboratory and country.
Keywords: Malaria; malaria vaccine; Plasmodium falciparum; Circumsporozoite protein; immunity.
Geliş Tarihi (Received): 13.07.2016 - Kabul Ediliş Tarihi (Accepted): 11.01.2017
GİRİŞ
Sıtma, halen d�nyada en fazla morbidite ve mortaliteye neden olan paraziter enfeksiyondur. Sıtmaya karşı etkin tedaviler g�n�m�zde kullanılmakta olup, hen�z hastalıktan tam olarak koruma sağlayan bir aşı mevcut değildir1-3.
Plasmodium t�rlerinin insanda enfeksiyona neden olan d�rt ana t�r� mevcuttur. Bunlar P.falciparum, P.ovale, P.malariae ve P.vivax'tır. İnsanlarda enfeksiyona neden olan beşinci bir t�r olan P.knowlesi aslında primatların sıtma etkeni olup insanlarda da zoonoz şeklinde sıtmaya neden olmaktadır. İki veya daha fazla Plasmodium t�r�yle kombine enfeksiyonlar da g�r�lebilmektedir. Sıtma etkenleri arasında en ağır klinik tabloyu oluşturan ve en fazla �l�me neden olan t�r P.falciparum'dur1-4.
D�nyada P.falciparum sıtması daha fazla g�r�lmekteyken, T�rkiye'de yerli olgularda P.vivax etkendir. �lkemizde cumhuriyetin kuruluşundan itibaren yoğun bir şekilde y�r�t�len m�cadele neticesinde yerli sıtma olgusu son yıllarda seyrektir1,2 fakat uluslararası seyahatin kolaylaşması sonucu son yıllarda �lkemizde ve b�lgemizde etkenin P.falciparum olduğu importe sıtma olguları daha sık g�r�lebilmektedir5-13.
Hastalığa karşı mevcut ila� alternatifinin sınırlı olmasının yanı sıra, var olan ila�lara da diren� gelişimi ve ila� yan etkileri nedeniyle kullanımının kısıtlanması; b�yle �nemli bir hastalık i�in neden halen etkili bir aşı olmadığı sorusunu akla getirmektedir. 1970'lerde atten�esporozoitlerin aşı olarak denenmesiyle başlayan �alışmalar, g�n�m�zde DNA ve protein aşı �alışmalarıyla devam etmektedir14.G�n�m�zde parazitin pre-eritrositer, eritrositer ve seks�el hayat evrelerine karşı etkili ve/veya bunların kombinasyonlarından oluşan aşılar geliştirilmeye �alışılmaktadır15.
Plasmodium'ların farklı hayat evrelerinde sentezlenen bir�ok antijen tek başına veya birbirleriyle kombine edilerek bir�ok aşı �alışmasında kullanılmıştır. İlk �alışmalarda atten�esporozoitlerle yapılan deneylerde bağışıklık elde edilmesi �zerine ilgi pre-eritrositer d�nem antijenleri �zerinde yoğunlaşmıştır. Pre-eritrositer d�nemin en �nemli antijenik yapısı da gerek sporozoitin gelişiminde, gerekse de invazyondan karaciğer evresine kadar olan d�nemde aktif rol oynayan Circumsporozoite proteindir (CSP)2.
Plasmodium'ların antijenik yapıları i�erisinde ilk tanımlanan CSP tek başına ve diğer antijenlerle beraber bir�ok aşı �alışmasında kullanılmıştır. Bu protein ilk olarak sivrisineklerin v�cudundaki ookistler i�erisindeki sporozoitlerde tespit edilmiştir. Dişi anofelin yumurta gelişimi i�in insandan kan emmesi esnasında dermis �zerine enjekte edilen sporozoit yapısında bu protein bulunmakta ve sporozoitin gelişiminde de �nemli rol oynamaktadır. CSP'nin yapısında bulunan N ve C terminali yapılarının parazitin enfekte edebildiği insan dışındaki t�rlerde de b�y�k oranda benzer olduğu bilinmektedir16,17.
Bu �alışmada P.falciparum CSP geninin klonlanıp, ekspresyon vekt�r�ne yerleştirilmesi ve sonrasındar rCSP proteininin ekspresyonu, optimizasyonu, saflaştırılması ve karakterizasyonu ama�lanmıştır.
GERE� ve Y�NTEM
CSP Geninin Elde Edilmesi
P.falciparum t�m genomik DNA'sından P.falciparum CSP geni i�in, spesifik primerler PfCSP F1 (5'-CACC ATG ATG AGA AAA TTA GCT AT-3') ve PfCSP R2 (5'-TTA ATT AAA GAA TAC TAA TAC-3')] kullanılarak PCR reaksiyonu hazırlandı. PCR d�ng�s� şartları; 94�C'de 5 dk denat�rasyonun ardından, 25 d�ng� 94�C'de 1 dk, 58�C'de 1.15 dk ve 72�C'de 1 dk ile bağlanma ve 72�C'de 30 dk uzama basamakları şeklinde d�zenlenmiştir.
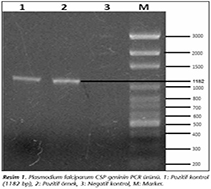
Elde edilen PCR �r�n� %0.8 etidyum brom�r i�eren %1.5 agaroz i�eren jelde marker eşliğinde y�r�t�lm�ş ve jel �zerindeki PCR �r�n�, Gel Logic 212 Pro Jel g�r�nt�leme cihazıyla g�r�nt�lenmiştir (Carestream, ABD).
CSP Geninin Klonlanması
Klonlama reaksiyonu, CloneJET PCR Cloning Kit (ThermoScientific, ABD)inde �nerilen y�nteme uygun olarak ger�ekleştirildi. Yapışkan u�lu klonlama protokol� uygulandıktan sonra elde edilen �r�n leligasyon reaksiyonu sayesinde CSP geni pJET vekt�r�ne klonlandı. Bu karışımdan 5μl alınarak buz �zerinde bekletilen mikrosantrif�j t�p�ndeki 100 �l kompetan OneShot� TOP10 Escherichia coli (Invitrogen, ABD) h�crelerine eklendi. Sonrasında mikrosantrif�j t�p�, 42�C'de 1 dk bekletilerek buz �zerine alındı ve �zerine 250 �l SOC medium eklendi. Daha sonra ampisilinli katı LB agar �zerine bu karışım ekildi ve 37oC'de bir gece ink�be edildi.
Transformasyon sonrası oluşan kolonilerin, rekombinant plazmit i�erip i�ermediğini tespit i�in PCR taraması yapıldı. Bunun i�in katı besiyerinden steril pipet ucuyla alınan her bir koloni, 25 μl'lik PCR tarama reaksiyon karışımına eklendi. PCR �r�n� agaroz jelde y�r�t�ld� ve g�r�nt�lendi.
Pozitif kolonilerden miniprep yapılarak CSP genini i�eren rekombinant plazmitler saflaştırıldı. Rekombinant plazmitler template olarak kullanılarak PCR yapıldı ve agaroz jelde g�r�nt�lenen P.falciparum CSP geninin varlığı doğrulandı. Ayrıca DNA dizi analizi yapılarak klonlamanın doğruluğu kesinleştirildi. DNA dizi analizi sonu�ları, Chromas v.1.45 programı ile http://blast.ncbi.nlm.nih.gov/ adresindeki BLAST (Basic Local Alignment Search Tool) programıyla veri tabanında mevcut olan P.falciparum dizileri ile karşılaştırılarak incelendi.
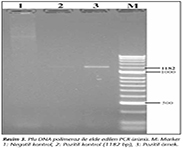
Elde edilen genin Champion� pET100 Directional TOPO� Expression Kit (ThermoScientific, ABD)vekt�r�ne yerleştirilebilmesi i�in Pfu DNA Polimeraz enzimi kullanılarak PCR reaksiyonu hazırlandı. Elde edilen PCR �r�n� agaroz jelde y�r�t�ld� ve g�r�nt�lendi.Protein ekspresyon ve p�rifikasyonu i�in Champion� pETDirectional TOPO� Expression Kit kullanıldı. P.falciparum CSP geninin pET100 vekt�r�ne subklonlanması �retici firma protokol�ne g�re yapıldı.
pET100 vekt�r�ne ligasyon ve transformasyon sonrasında oluşan kolonilerin, rekombinant plazmit i�erip i�ermediğini anlamak i�in PCR taraması yapıldı ve CSP geninin pET100 vekt�r�ne transformasyonu sonrası PCR taraması ile pozitifliği belirlenen koloni LB sıvı besiyerine ekilerek miniprep prosed�r� uygulandı. PCR y�ntemi ile rekombinant plazmit varlığı doğrulandı. DNA dizi analizi ile varlığı kesinleştirilen rekombinant plazmit, rCSP �retimi i�in BL21 Star E.coli h�crelerine transforme edildi.
rCSP Ekspresyonu
Transformasyon �r�n�n�n 500'er �l'si 50 ml'lik 10 ml sıvı LB i�eren 2 adet t�pe aktarılarak ikiye b�l�nd�. Sıvı besiyerleri 37�C'de OD600 0.5-0.8 olana kadar yaklaşık 3 saat ink�be edildi. Protokol sonunda negatif �rnekle birlikte, alınan diğer �rnekler -20�C'de saklandı. Bu �rnekler rCSP analizi aşamasında kullanıldı.
Mini-PROTEAN� Tetra Cell Systems (Bio-Rad, ABD) SDS-PAGE'de y�r�t�len proteinler Trans-Blot� Turbo� Transfer System Western Blot (Bio-Rad, ABD) sistemle nitrosel�loz membrana transfer edildi. Bloklama ve Anti-HisG-HRP antikor (İnvitrogen, ABD) ink�basyonu sonrası rekombinant proteine ait bantlar DAB tablet y�ntemi ile tespit edildi.
rCSP'nin Saflaştırılması ve Endotoksinlerinden Arındırılması
Rekombinant protein ekspresyonu 3.5 saat 0.1 mM IPTG ile ind�klenerek optimize edildi. rCSP'nin saflaştırılması, Protein Purification System Kit (ProBond, ABD) prosed�r�ne uygun olarak yapıldı. Saflaştırılmış rCSP'nin doğruluğu SDS-PAGE sonrası Western blotta Anti-HisG-HRP antikor ve DAB ile g�sterildi.
Saflaştırılan rCSP'denen dotoksinlerin ayrıştırılması "ToxinEraser� Endotoxin Removal Kit (Genscript, ABD)" kullanılarak �retici firma �nerisine g�re yapıldı. Saflaştırılan ve endotoksinleri uzaklaştırılan rCSP'nin endotoksin seviyesi Pierce LAL Chromogenic EndotoxinQuantitationKit (Thermo Scientific, ABD) kullanılarak �l��ld�.
rCSP'nin Aminoasit Dizilimi ve 3 Boyutlu Yapısının Elde Edilmesi
DNA dizi analizi yapılarak elde edilen P.falciparum CSP gen dizisi kullanılarak http://www.ebi.ac.uk/Tools/st/emboss_transeq/adresindeki program ile rCSP'ninaminoasit dizilimi elde edildi. http://www.sbg.bio.ic.ac.uk/phyre2/html/page.cgiid=index adresindeki J mol 14.2.15_2015.07.09 programı kullanılarak rCSP'nin 3 boyutlu şekli elde edildi.
BULGULAR
P.falciparum genomik DNA'sından CSP spesifik primerler kullanılarak PCR kurularak 1.182 bp b�y�kl�ğ�nde PCR �r�n� elde edilmiştir (Resim 1).
PCR ile elde edilen P.falciparum CSP geni pJET vekt�r�ne klonlandı. Klonlamanın doğruluğunu g�stermek amacıyla rekombinant plazmitin DNA dizi analizi yapıldı. DNA dizi analizi ile gen klonlamasının doğruluğu ve CSP geninin DNA dizisi tespit edildi (Resim 2). �alışmada elde edilen1.182 bp b�y�kl�ğ�ndeki P.falciparum CSP geni GenBank'a KT315396 numarası ile kaydedilmiştir.
pET100 ekspresyon vekt�r�ne plazmitin yerleştirilebilmesi i�in Pfu DNA polimeraz enzimi ile �oğaltılan 1.182 bp b�y�kl�ğ�ndeki CSP geni pJET vekt�r�nden subklonlama ile pET100 plazmitine yerleştirilmiştir (Resim 3).
pET100 vekt�r�ne P.falciparum CSP geninin yerleştirilmesi ile oluşturulan rekombinant plazmite pET100PfCSP adı verildi. Rekombinant pET100PfCSP plazmiti, BL21 star E.coli h�crelerine transformasyonu sonrasında IPTG ile ind�klenerek rekombinant protein ekspresyonu uyarıldı. Elde edilen rCSP, SDS-PAGE ve Western Blot y�ntemiyle Anti-HisG-HRP antikor ve DAB ile g�sterilmiştir (Resim 4).
P.falciparum CSP gen dizisi kullanılarak 393 aminoasitten oluşan rCSP yapısı elde edildi (Resim 5). Bu �alışmada elde edilen rCSP i�yapısında merkezi b�lgede toplam 37 NANP epitopu (Asn-Ala-Asn-Pro) bulunmaktadır. Merkezi b�lgede tek başına 3 NANP-NVDP epitop tekrarından sonra 15 NANP tekrarı ve arada bulunan bir NVDP epitopunun ardından tekrar 19 NANP epitop tekrarı olduğu tespit edilmiştir. rCSP yapısında toplam 4 adet birbirinden bağımsız NVDP epitopu bulunduğu g�r�lm�şt�r.
P.falciparum CSP gen dizisi kullanılarak rCSP'nin 3 boyutlu yapısı elde edilmiştir (Resim 6).
TARTIŞMA
P.falciparum, sıtmaya neden olan parazitler i�erisinde en sık karşılaşılan t�r olmanın yanında en ağır klinik tabloyu oluşturan ve en fazla �l�me neden olan etkendir. �lkemizde sıtma etkeni olarak P.vivax g�r�lmekteyken, son yıllarda uluslararası seyahatin kolaylaşması, g��ler, savaşlar ve �ğrenci değişim programları gibi etkenlere bağlı olarak P.falciparum ile ortaya �ıkan sıtma olgularının sayısı da giderek artmaktadır5-13. Aşı �alışmalarına en fazla konu olan sıtma etkeni P.falciparum'dur16.
Sıtmaya karşı aşı geliştirme �alışmaları 1970'li yıllarda başlamıştır. İlk olarak kullanılan radyasyonla atten�e edilmiş sporozoitleri taşıyan sivrisineklere maruz bırakılan kişilerde kısmi bağışıklık elde edilmiştir14. Gamma ışınlarıyla zayıflatılmış sporozoitler aşı olarak kısıtlı bir bağışıklık oluşturmuştur. Busporozoitlerin bağışıklık oluşturabilmesi i�in binden fazla sivrisinek ısırığı gereklidir ve seri �retiminde g��l�kler yaşanmaktadır. �nceki �alışmalarda elde edilen başarılı sonu�lar sayesinde g�n�m�zde bu y�ndeki �alışmalar tekrar ilgi odağı olmuştur18-20.
RTS,S aşısı DS� g�kkuşağı tablosuna g�re Faz III �alışmalarına ulaşabilmiş tek sıtma aşısıdır. Bu aşıda 19 NANP epitop tekrarı bulunmaktadır. Aynı zamanda Hepatit B y�zey antijenine bağlanmış olan CSP'nin C terminalini de i�ermektedir. RTS,S'de adjuvan olarak ise AS01E kullanılmıştır2. RTS,S'in Faz III �alışmaları sonucu elde edilen verilere g�re, 5-17 aylık s�t �ocuklarında yapılan ilk doz aşılamayı takiben 18 ay sonra ikinci bir doz uygulanmasıyla, sıtma olgu sayısını %36 oranında azalttığı bulunmuştur. İlk doz aşılamada 6-12 haftalık olan infantlarda ise %26 oranında koruma sağlandığı tespit edilmiştir. Bunun yanı sıra aşının etkinliğinin her iki grupta da zamanla azaldığı g�zlenmiştir. Aşının etkinliğinin değerlendirilmesinde %80 civarında insektisit ve cibinlik gibi diğer koruma fakt�rlerinin de mevcut olduğu g�z �n�nde bulundurulmuştur. RTS,S saha �alışmaları, sıtmanın en fazla �l�me neden olduğu Afrika'da ve yine en fazla �l�me neden olduğu grup olan 5 yaş altı �ocuklar �zerinde yapılmıştır. 2013 yılında yapılan bir araştırmanın sonu�larına bakıldığında RTS,S'in 4 yıl sonunda koruma oranı %16.8 olarak bulunmuştur. Afrika'da geniş katılımlı bir �alışmada 6 ila 12 haftalık 6537 infantın dahil edilmesiyle yapılan Faz III �alışmasında RTS,S sıtmaya karşı yaklaşık %30 oranında bir koruma sağlamıştır. Afrika'nın 11 farklı b�lgesinde y�r�t�len ve 4453 �ocuk �zerinde yapılan bir diğer araştırmada sıtmanın d�ş�k transmisyonunun g�r�ld�ğ� b�lgelerde %60 koruma, orta derecede transmisyonun olduğu b�lgelerde %41 koruma ve y�ksek transmisyonun olduğu b�lgelerde ise %4 koruma g�zlenmiştir21-23.
Aşının �reticisi olan Glaxo Smith Kline (GSK, İngiltere) firması Haziran 2014'de Avrupa İla� Ajansı (AİA)'na ruhsat almak �zere resmen başvurmuştur. GSK, AİA'nın değerlendirme sonucuna g�re, RTS,S'in Temmuz 2015 itibariyle onaylandığını; 2017 yılında ise son olarak DS� tarafından kullanıma sunulup sunulmayacağına karar verileceğini duyurmuştur. Elimizdeki bu veriler ışığında bir değerlendirme yapıldığında, CSP bazlı RTS,S'in, sıtmaya karşı ılımlı bir koruma sağladığı; bu koruyuculuğun %100 olmadığı ve bu konuda �n�m�zdeki yıllarda daha detaylı �alışmalar yapılarak, daha etkili aşı form�lasyonlarının geliştirilmesi gerektiği sonucuna ulaşabiliriz. Ayrıca aşı adayı olabilecek hedef antijenler i�inde bir�ok molek�l olmasına karşın en �nemli molek�l de CSP olarak g�r�lmektedir.
�alışmamızda kullanılan P.falciparum CSP geninin b�y�kl�ğ� 1.182 bp'dir. http://www.ncbi.nlm.nih.gov/nuccore adresinde mevcut bulunan CSP gen dizilerinin b�y�kl�ğ� 1.032-2.337 bp arasındadır. GenBank'ta AB502850.1 (Tanzanya izolatı) kayıt numaralı gen ile �alışmamızda izole edilenve KT315396 numara ile kayıt edilen gen %100 aynı baz dizilimine sahiptir.
Pre-eritrositer d�nem aşılarında, CSP'nin merkezinde bulunan ve proteinin ana karakterini belirleyen NANP tekrarlarının �nemi dikkate alınarak aşı �alışmalarında kullanılmıştır2,24. NANP epitoplarının; CSP'nin yapısında doğal olarak bulunduğu şekilde ve/veya sentetik şekilde 3 ila 19 tekrar halinde aşı �alışmalarında etkinliği araştırılmıştır. Bu epitopun aşı �alışmalarında stratejik bir hedef olarak se�ilmesi olduk�a ger�ek�i ve akılcı bir yaklaşım olarak g�n�m�ze kadar kabul g�rm�şt�r25,26.
CSP'ye karşı oluşan humoral bağışıklıkta NANP epitop tekrarı �nemli bir rol oynamaktadır. Malawi'de NANP epitop tekrarının polimorfizmi �zerine yapılan bir �alışmada 98 farklı izolat kullanılmış ve sonu�ta 20 farklı epitop tespit edilmiştir. RTS,S yapısında 19 NANP tekrarı bulunduğunun bilinmesine rağmen farklı izolatlarda olduk�a değişken sayılarda NANP tekrarı bulunduğu bildirilmiştir27-29. Bizim �alışmamızda kullanılan izolattan elde edilen CSP'deki NANP epitopu tekrar sayısı 37 olarak tespit edilmiştir. Literat�rdeki bilgiler ışığında, kullanmış olduğumuz rCSP'deki NANP tekrarının konak imm�nitesinde B ve T lenfosit yanıtını uyararak yapılacak �alışmalarda aşı etkinliğine olumlu katkılarının olabileceğini d�ş�nmekteyiz.
P.falciparum'un pre-eritrositer d�neme ait en �nemli antijenik yapılarından olan CSP'in rekombinant olarak �retilip, aşı adayı olarak tasarlandığı bu �alışmada; P.falciparum genomik DNA'sı kullanılarak; spesifik primerlerle CSP gen b�lgesi PCR ile �oğaltılıp daha sonra plazmite klonlanmıştır. Rekombinant plazmit BL21 h�crelerinde eksprese edilmiştir. Eksprese edilen rekombinant protein saflaştırılarak, endotoksinlerinden arındırılmıştır. rCSP'nin etkinliğinin farklı deney hayvanlarında araştırılabilmesi i�in; rekombinant protein ekspresyon optimizasyonu �alışmalarının yanı sıra, daha y�ksek miktarlarda elde edilebilmesi gerekmektedir30.
G�n�m�zde halen milyonlarla ifade edilen olgu sayısı ve y�zbinlerle ifade edilen can kayıplarına rağmen, sıtmaya karşı etkili bir aşı olmaması ve mevcut ila�ların hepsine karşı bildirilen diren�, bu alanda yapılan ve yapılması planlanan �alışmaları daha da �nemli hale getirmektedir.
Bu �alışma sonrasında, farklı modifikasyonlarla elde edilecek verilerin geliştirilmesi ve diğer y�ksek organizmalı deney hayvanlarında enfeksiyona karşı etkinliğinin araştırılması ile sıtmaya karşı aşı �alışmalarına �nemli bir katkı sağlanmış olunacaktır.
KAYNAKLAR
- Yazar S, Kuk S, Miman �, Saygı G. Saygı'nın Temel Tıbbi Parazitoloji'si. 2016, Erciyes �niversitesi Yayını, Kayseri.
- �zcel MA, �zbel Y, Ak M (ed). �zcel'in Tıbbi Parazit Hastalıkları. 2007, T�rkiye Parazitoloji Derneği Yayını No: 22. Meta Basım Bornova, İzmir.
- Altıntaş K, Tıbbi Parazitoloji. 2002, Mn Medikal Nobel Yayını, Ankara.
- Cox-Singh J. Zoonotic malaria: Plasmodium knowlesi, an emerging pathogen. Curr Opin İnfect Dis 2012; 25(5): 530-6.
- Uyar Y, İnan� T, Sahin S, Kuk S, Yazar S. 2001-2013 Yılları Arasında Kayseri'de Sıtma Epidemiyolojisi. Turkiye Parazitol Derg 2015;39:86-9.
- Bayındır Y, Aycan �M, Atambay M, Karaman �, Aydoğdu İ. Malatya'da Uganda K�kenli İlk Falciparum Sıtması: İki Olgu. Turkiye Parazitol Derg 2005; 29: 157-9.
- Alver O, Yılmaz E, Ak�ağlar S, T�re O. Bursa'da Sıtma. Turkiye Parazitol Derg 2007; 31: 249-55.
- Karaman �, Atambay M, Yaşar S ve ark. Malatya'da son yedi yıl i�indeki sıtma olguları. Turkiye Parazitol Derg 2007; 31: 245-8.
- Parlak E, Ert�rk A, �ayır Y, Parlak M. Sporadik bir b�lgede: D�rt import sıtma olgusu. Turkiye Parazitol Derg 2013; 37: 161-4.
- �elik T, K�lgelier S. Adıyaman'da 2000-2011 yılları arasında aktif ve pasif s�rveyans ile saptanan sıtma olguları. Turkiye Parazitol Derg 2012; 36: 204-7.
- Altun HU, G�l YK, Vudalı E ve ark. Uganda kaynaklı Plasmodium falciparum sıtması. Turkiye Parazitol Derg 2013; 37: 229-32.
- Cetinkol Y, Yıldırım AA. Ordu ilinde 2002-2011 yılları arasında sıtma epidemiyolojisi. Turkiye Parazitol Derg 2013; 37: 69-72.
- G�venT, Eser FC, Yılmaz GR, G�ner R, Taşyaran MA. Seyahat ilişkili P.falciparum sıtması: D�rt olgu. Turkiye Parazitol Derg 2013; 37: 225-8.
- Clyde DF. Immunization of man against falciparum and vivax malaria by use of attenuated sporozoites. Am J Trop Med Hyg 1975; 24(3): 397-401.
- Richie TL, Saul A. Progress and challenges for malaria vaccines. Nature 2002; 415: 694-701.
- Doud MB, Koksal AC, Mi LZ, et al. Unexpected fold in the circumsporozoite protein target of malaria vaccines. Proc Natl Acad Sci 2012; 109(20): 7817-22.
- Chakravarty S, Cockburn IA, Kuk S, et al. CD8+ T lymphocytes protective against malaria liver stages are primed in skin-draining lymph nodes. Nature Medicine 2007; 13: 1035-41.
- R�nia L, Gr�ner AC, Mauduit M, Snounou G. Vaccination using normal live sporozoites under drug treatment. Methods Mol Biol 2013; 923: 567-76.
- Roestenberg M, McCall M, Hopman J, et al. Protection against a malaria challenge by sporozoite inoculation. N Engl J Med 2009; 361(5): 468-77.
- Luke TC, Hoffman SL. Rationale and plans for developing a non-replicating, metabolically active, radiation-attenuated Plasmodium falciparum sporozoite vaccine. J Exp Biol 2003; 206(Pt 21): 3803-8.
- Agnandji ST, Lell B, Fernandes JF, et al. A phase 3 trial of RTS,S/AS01 malaria vaccine in African infants. N Engl J Med 2012; 367(24): 2284-95.
- Bejon P, White MT, Olotu A, et al. Efficacy of RTS,S malaria vaccines: individual-participant pooled analysis of� phase 2 data. Lancet Infect Dis 2013; 13(4): 319-27.
- Olotu A, Fegan G, Wambua J, et al. Four-year efficacy of RTS,S/AS01E and its interaction with malaria exposure. N Engl J Med 2013; 368(12): 1111-20.
- Graves PM, Gelband H. Vaccines for preventing malaria (pre-erythrocytic). The Cochrane Database of Systematic Reviews. 2009; Issue 1.
- Zavala F, Tam JP, Hollingdale MR, et al. Rationale for development of a synthetic vaccine against Plasmodium falciparum malaria. Science 1985; 228(4706): 1436-40.
- Espinosa DA, Gutierrez GM, Rojas-L�pez M, et al. Proteolytic Cleavage of the Plasmodium falciparum Circumsporozoite protein is a target of protective antibodies. J Infect Dis 2015; 212(7): 1111-9.
- Bowman NM, Congdon S, Mvalo T, et al. Comparative population structure of Plasmodium falciparum circumsporozoite protein NANP repeat lengths in Lilongwe, Malawi. Sci Rep 2013; 3: 1990.
- Zeeshan M, Alam MT, Vinayak S, et al. Genetic variation in the Plasmodium falciparum circumsporozoite protein in India and its relevance to RTS,S malaria vaccine. PLoS One 2012; 7(8): e43430.
- Rich SM, Ferreira MU, Ayala FJ. The origin of antigenic diversity in Plasmodium falciparum. Parasitol Today 2000; 16(9): 390-6.
- Recombinant protein production optimization. Available from: URL:� http://www.genscript.com/gsfiles/techfiles/Optimizing_conditions_for_recombinant_soluble_protein_production_in_E_coli.pdf.
İletişim (Correspondence):
Dr. Yunus Uyar,
T�rk Kızılayı Kan Bağış Merkezi,
Kayseri, T�rkiye.
Tel (Phone): +90 505 681 5740,
E-posta (E-mail): dryunusuyar@yahoo.com