Solid Organ Nakli Alıcılarında CMV Antijenemi Testi ve CMV-DNA PCR Sonu�larının Karşılaştırılması*
Comparison of the CMV Antigenemia Test and CMV-DNA PCR Results in Solid Organ Transplant Recipients
Emre �ZKARATAŞ1, �. Alpay �ZBEK1, Vildan AVKAN OĞUZ2, A. Arzu SAYINER1
1 Dokuz Eyl�l �niversitesi Tıp Fak�ltesi, Tıbbi Mikrobiyoloji Anabilim Dalı, İzmir.
1 Dokuz Eylul University Faculty of Medicine, Department of Medical Microbiology, Izmir, Turkey.
2 Dokuz Eyl�l �niversitesi Tıp Fak�ltesi, Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı, İzmir.
2 Dokuz Eylul University Faculty of Medicine, Department of Infectious Diseases and Clinical Microbiology, Izmir, Turkey.
* Bu �alışma, 8. Ulusal Molek�ler ve Tanısal Mikrobiyoloji Kongresi (4-7 Haziran 2014, Ankara)'nde poster olarak sunulmuştur.
�Z
Sitomegalovirus (CMV) enfeksiyonu, solid organ transplant alıcılarında sık karşılaşılan �nemli viral enfeksiyonlardan biridir. Bu grup hastada, CMV replikasyonunu saptayan tanı testlerinin yaygın kullanımına karşın, sonu�ların yorumlanmasında, �zellikle d�ş�k viral y�k�n klinik anlamı konusunda fikir birliği bulunmamaktadır. Bu �alışmada, Dokuz Eyl�l �niversitesi Hastanesi Merkez Laboratuvarında, 2011-2013 yılları arasında karaciğer ve b�brek alıcılarında CMV pp65 antijenemi testi ve plazmada kantitatif CMV-DNA ger�ek zamanlı polimeraz zincir reaksiyonu (kPCR) y�ntemiyle elde edilen sonu�lar karşılaştırılmış ve iki y�ntem arasındaki korelasyon değerlendirilerek, antijenemi pozitifliğine denk gelen viral y�k d�zeyi belirlenmiştir. �alışmada, pp65 antijenemi ve CMV-DNA kPCR test sonucu olan �rnekler retrospektif olarak incelenmiştir. Aynı hastaya ait antijenemi ile CMV-DNA kPCR testi arasında 48 saate kadar s�re olan �rnekler �alışmaya dahil edilmiştir. Korelasyon, regresyon ve ROC analizleri i�in SPSS yazılımı v15.0 kullanılmıştır. �alışmamızda, 36'sı karaciğer, 64'� b�brek transplantasyonu yapılan 100 hastaya (59 erkek, 41 kadın; yaş aralığı: 16-71, ortalama yaş: 46 � 13 yıl) ait 217 �rneğin sonu�ları değerlendirilmiştir. Hastaların %80'i CMV IgM negatif, IgG pozitif; %1'i CMV IgG ve IgM pozitif; %2'si CMV IgM ve IgG negatif olup, 17 hastanın seroloji sonu�larına ulaşılamamıştır. �rneklerin 102'sinde (%47) CMV pp65 antijenemi ve CMV-DNA negatif; 37 (%17)'sinde ise her iki test sonucu da pozitif bulunmuştur. CMV IgM ve IgG antikorları pozitif olan tek olgunun değerlendirilen tek �rneğinde antijenemi ve CMV-DNA testleri negatiftir.� Antijenemi negatif/CMV-DNA kPCR pozitif �rnek sayısı 78 iken, antijenemi pozitif/kPCR negatif saptanan �rnek yoktur. Her iki test sonucu pozitif olan ve kantite edilebilen �rneklerde (n= 35), antijenemi ve kPCR ortalama değerleri sırasıyla; 23 pozitif h�cre/200.000 l�kosit (aralık: 1-230 pozitif h�cre) ve 12.595 kopya/ml (aralık: 180-106.311 kopya/ml) olarak saptanmıştır. Her iki test ile pozitif saptanan �rnekler arasındaki korelasyon anlamlı bulunmuştur (r= 0.785). ROC analizi, plazmada 205 kopya/ml CMV viral y�k�n�n ≥ 1 antijen pozitif h�cre/200.000 l�kosite karşılık geldiğini g�stermiştir (duyarlılık: %91.7, �zg�ll�k: %90.3). CMV-DNA PCR pozitif, pp65 antijenemi negatif bulunan �rnekler, kPCR y�nteminin analitik a�ıdan antijenemiye g�re daha duyarlı olması ile a�ıklanabilir. Antijenemi pozitif/PCR negatif �rneğin olmaması bu durumu desteklemektedir. ROC analizi, CMV-DNA kPCR sonucu 205 kopya/ml altındaki bir �rneğin, pp65 antijeni negatif olarak kabul edilebileceğini g�stermiştir. Belirlenen bu değer, �alışmada incelenen hasta grubu ve kullanılan testler i�in ge�erli olup, grup ve testlere bağlı olarak değişiklik g�sterebilir.
Anahtar s�zc�kler: CMV; DNA; antijenemi testi; polimeraz zincir reaksiyonu; organ transplantasyonu.
ABSTRACT
Cytomegalovirus (CMV) infection is among the most common important viral infections in solid organ transplant (SOT) recipients. Diagnostic tests for detecting CMV replication are widely used for this group of patients, however there is no clear agreement on the cut-off levels for interpretation of clinical decisions especially when the low level of viral load is detected. In this study, CMV pp65 antigenemia test results were compared with plasma CMV-DNA levels detected by quantitative real-time polymerase chain reaction (qPCR) in samples of kidney and liver transplant recipients in the Central Laboratory of Dokuz Eylul University Hospital between 2011 and 2013, and the correlation between these two tests and viral load equivalent to antigenemia positivity were determined. In the study, pp65 antigenemia and CMV-DNA qPCR results were evaluated retrospectively. The samples from the same patients were included if the time between antigenemia and CMV-DNA qPCR tests were less than 48 hours. SPSS v15.0 was used for correlation, regression and ROC curve analysis. The results of the 217 samples collected from 100 patients (59 male, 41 female; age range: 16-71, mean age: 46 � 13 years), 36 liver and 64 kidney recipients were evaluated in the study. Of the patients 80% were CMV IgM negative, IgG positive; 1% was CMV IgG and IgM positive; 2% were CMV IgM and IgG negative, while for 17 patients serological results could not be reached. CMV pp65 antigenemia and CMV-DNA were both negative in 102 (47%) samples, while both were positive in 37 (17%) samples. The single sample from a case with CMV IgM and IgG positivity yielded negative results for both antigenemia and CMV-DNA tests. In 78 samples antigenemia were negative and CMV-DNA qPCR were positive, while there were no samples with antigenemia positive and qPCR negative. Mean values of antigenemia and qPCR tests were 23 positive cells/200.000 leukocytes (range: 1 to 230 positive cells) and 12.595 copies/ml (range: 180 to 106.311 copies/ml), respectively. There was a significant correlation between antigenemia and qPCR results among the samples that were positive by both assays (r= 0.785). ROC curve analysis showed that CMV viral load of 205 copies/ml in plasma corresponds to ≥ 1 pp65 antigen positive cells per 200.000 leukocytes (sensitivity: 91.7%, specificity: 90.3%). Higher analytical sensitivity of qPCR test can be explained by the results of CMV-DNA PCR positive and antigenemia negative samples. Non-existence of samples with antigen positive and PCR negative results supported this finding. ROC analysis showed that any sample with CMV-DNA qPCR result less than 205 copies/ml, could be accepted as pp65 antigenemia negative. This viral load value is valid only for the studied patient group and assays, therefore could be changed according to study population and tests.
Keywords: CMV; DNA; antigenemia test, polymerase chain reaction; organ transplantation.
Geliş Tarihi (Received): 05.08.2015 • Kabul Ediliş Tarihi (Accepted): 10.12.2015
GİRİŞ
Sitomegalovirus (CMV) enfeksiyonu, solid organ nakli alıcılarında mortalite ve morbiditeye yol a�an� viral enfeksiyonlar arasında en sık karşılaşılanıdır. Bu hastalarda CMV replikasyonunun etkisi, �zg�l organ tutulumundan (akciğer, gastrointestinal sistem, karaciğer, b�brek ve merkezi sinir sistemi) yaygın CMV hastalığına kadar değişkenlik g�sterebilmekte, nakledilen organın kaybına yol a�abilmektedir. Hastaların klinik y�netiminde, aktif CMV enfeksiyonunun �nlenmesi ve tedavisi �nemli bir yer tutmaktadır. Transplant alıcılarında CMV viremisi, nadir g�r�len belirli bir organla sınırlı enfeksiyonlar dışında, genellikle CMV hastalığından �nce saptanır ve gerek enfeksiyon tanısı gerekse preemptif tedavi kararının alınmasında �nemli bir parametredir. Preemptif tedavinin etkinliği, CMV replikasyonunun erken aşamalarını saptayabilen uygun tanısal testlerin (pp65 antijenemi, CMV-DNA PCR) kullanımına bağlıdır1. CMV enfeksiyonunu saptayan testlerin yaygın kullanılmasına karşın, sonu�ların yorumlanmasında, �zellikle d�ş�k CMV viral y�k�n�n klinik anlamı konusunda sıkıntılar vardır2. Tedaviye başlamak i�in eşik değeri d�ş�k tutmak gereksiz tedavilere, y�ksek tutmak ise tedavinin gecikmesi ve dolayısıyla CMV hastalığının gelişmesine yol a�abilir.
Periferik kan l�kositlerinde CMV pp65 (UL83) proteininin saptanması (pp65 antijenemisi), CMV enfeksiyonunun izlenmesinde pop�ler bir y�ntem olmakla birlikte, yoğun iş g�c� gerektirmesi, sonu�ların değerlendirilmesinin deneyim gerektirmesi ve subjektif olması, �ok sayıda �rneğin �alışılmasına imkan sağlamaması gibi dezavantajları vardır.� H�creler �rnek alımından sonra altı saat i�inde ayrılmış, sayılmış, lama aktarılmış ve fikse edilmiş olmalıdır. Hastadan elde edilen mutlak n�trofil sayısı 2 x 106 /ml'nin altında olduğunda test g�venilir değildir1,3,4.
Tanı ve izlemde kullanılabilecek diğer test, kanda viral y�k�n kantitatif n�kleik asit testleri ile belirlenmesidir. CMV-DNA kantitatif ger�ek zamanlı polimeraz zincir reaksiyonu (kPCR) y�ntemi son yıllarda yaygın olarak kullanılmaktadır1,2. Bu y�ntem geniş dinamik aralıkta kantitasyon yapabilir ve standardizasyon i�in uygundur. Otomatize n�kleik asit ekstraksiyon y�ntemlerinin teste eklenmesi, sonu�ların daha g�venilir ve tekrarlanabilir olmasını sağlamış, test s�resini kısaltarak rutin uygulamada testin kullanımını yaygınlaştırmıştır. PCR esaslı testler, antijenemi testinden daha duyarlıdır; ancak y�ksek duyarlılık, klinik anlamı tartışmalı d�ş�k viral repikasyonların da saptanmasına yol a�maktadır. Uluslararası CMV-DNA standardı geliştirilmiş olmasına rağmen, kullanılan kPCR testleri arasındaki farklılıklar, laboratuvarlar arası standardizasyonun sağlanmasını g��leştirmekte ve klinik anlamı belirlenmiş eşik değerler konusunda karar verilmesini zorlaştırmaktadır5,6. Bu �alışmada, Dokuz Eyl�l �niversitesi Hastanesi Merkez Laboratuvarında 2011-2013 yılları arasında solid organ nakli alıcılarında vireminin saptanması i�in l�kositlerde pp65 antijenemi testi ve plazmada CMV-DNA kPCR y�ntemiyle elde edilen sonu�lar karşılaştırılmış ve iki y�ntem arasındaki korelasyon değerlendirilerek, antijenemi pozitifliğine denk gelen viral y�k d�zeyi belirlenmiştir.
GERE� ve Y�NTEM
�alışmamızda; Dokuz Eyl�l �niversitesi Hastanesi Merkez Laboratuvarında 2011-2013 yılları arasında solid organ nakli alıcılarında (karaciğer ve b�brek transplantasyonu) pp65 antijenemi ve CMV-DNA kPCR testi birlikte �alışılmış �rnekler retrospektif olarak değerlendi. Aynı hastaya ait antijenemi ile CMV-DNA kPCR testi arasında maksimum 48 saate kadar s�re olan �rnekler �alışmaya dahil edildi. Alıcıların CMV enfeksiyonu a�ısından risklerini belirlemek amacıyla, transplantasyon �ncesi CMV antikor test sonu�ları retrospektif olarak incelendi. �alışma i�in Dokuz Eyl�l �niversitesi Girişimsel Olmayan Araştırmalar Etik Kurulu'ndan onay alındı.
CMV pp65 (UL83) antijenemi testi, indirekt imm�nofloresans y�ntemi ile periferik kan l�kositlerinde viral matriks fosfoproteinini (pp65) saptamak i�in, �reticinin (CINAKit, Argene�, Fransa)� talimatlarına uygun olarak yapıldı. Talimatlarda belirtildiği gibi her �rnekte l�kosit sayımı yapıldı ve 2x106/ml h�cre sayısı sağlanarak lama aktarım (sitospin) basamağına ge�ildi. İstenen h�cre sayısına ulaşılamayan �rnekler �alışmaya alınmadı. Preparatlar, floresans mikroskobunda değerlendirildi ve sonu�lar 200.000 periferik kan l�kositi başına pozitif h�cre sayısı olarak verildi.
Plazmada CMV viral y�k testi, ger�ek zamanlı PCR y�ntemiyle (Artus� CMV QS-RGQ Kit, QIAGEN, Almanya) �reticinin talimatlarına uygun olarak ger�ekleştirildi. İnternal kontrol her �rneğe ekstraksiyondan �nce eklendi. Kitin analitik duyarlılığı 43 kopya/ml (70 IU/ml), kantitasyon aralığı 80-1 x 108 kopya/ml olup, kit i�inde, yalancı negatifliklerin saptanabilmesi i�in internal kontrol bulunmaktadır.
İki y�ntemin test sonu�larının uyumu, korelasyon analizi ile değerlendirildi, antijenemi pozitifliğine karşılık gelen viral y�k d�zeyi ise ROC analizi ile belirlendi. Korelasyon analizi i�in, pozitif sonu� elde edilen antijenemi ve CMV-DNA (log10) verileri kullanıldı ve CMV-DNA testinde kantitasyon alt sınırından daha d�ş�k değerler (< 80 kopya/ml) değerlendirmeye alınmadı. Korelasyon analizinden sonra lineer regresyon analizi yapıldı. Alıcı işletim karakteristik eğrisi (ROC) analizinde antijenemi y�nteminin pozitifliği esas alınarak (≥ 1 pozitif h�cre/200.000 h�cre), buna karşılık gelen plazma CMV-DNA y�k� hesaplandı ve antijenemi testinin pozitifliği esas alınarak, CMV-DNA kPCR testinin duyarlılık, �zg�ll�k, pozitif (PPD) ve negatif (NPD) prediktif değerleri belirlendi. Bu değerlendirmelerde t�m CMV-DNA pozitiflikleri (80 kopya/ml değerinin altındaki ve �st�ndeki sonu�lar) PCR pozitif olarak gruplandırıldı. Analizler i�in� SPSS yazılımı (versiyon 15; SPSS Inc., ABD) kullanıldı.
BULGULAR
�alışmamızda; kriterlere uygun 100 solid organ nakli alıcısının 217 �rneğine ait sonu�lar retrospektif olarak incelenmiştir. Olguların 59 (%59)'u erkek (22 karaciğer, 37 b�brek transplantasyonu), 41 (%41)'i kadın (14 karaciğer, 27 b�brek transplantasyonu) olup, yaşları 16-71 (ortalama yaş: 46 � 13) yıl arasında değişmektedir.
Hastaların transplantasyon �ncesi CMV serolojileri değerlendirildiğinde; 80 (%80) hastada CMV IgM negatif, CMV IgG pozitif; bir (%1) hastada CMV IgG ve CMV IgM pozitif; iki (%2) hastada CMV IgM ve IgG negatif saptanmış, 17 (%17) hastanın seroloji sonu�larına ulaşılamamıştır. Bu sonu�lara g�re transplantasyon alıcılarının en az %80'i d�ş�k riskli gruptadır.�
CMV antijenemi ve CMV-DNA PCR testleri karşılaştırılarak elde edilen sonu�lar Tablo I'de g�sterilmiştir. �rneklerin %64 (139/217)'�nde sonu�lar uyumludur; her iki test sonucu 67 hastaya ait 102 (%47) �rnekte negatif, 23 hastaya ait 37 (%17) �rnekte pozitif saptanmıştır. Her iki test sonucu pozitif olan ve kantite edilebilen �rneklerde (n=35), antijenemi ve kPCR ortalama değerleri sırasıyla; 23 pozitif h�cre/200.000 h�cre (aralık: 1-230 pozitif h�cre/200.000) ve 12.595 kopya/ml (aralık: 180-106.311 kopya/ml) olarak bulunmuştur. Antijenemi y�ntemiyle pozitiflik saptanan 2 hastaya ait 2 �rnekte CMV-DNA değeri kantitasyon alt sınırının altındadır (< 80 kopya/ml).
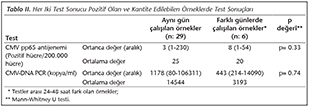
Her iki test sonucu kantite edilebilen 35 �rnek �iftinden, 29'unda antijenemi ve PCR testleri aynı g�n, 6'sında farklı g�nlerde �alışılmıştır. Testlerin aynı g�n veya farklı g�nlerde �alışılmasına g�re elde edilen sonu�lar Tablo II'de �zetlenmiştir. Buna g�re gruplar arasında her iki testin kantitatif değerleri a�ısından istatistiksel olarak anlamlı fark yoktur (p≥ 0.05).
pp65 anijenemi testi negatif 43 hastaya ait 78 �rnekte (%36), CMV-DNA pozitif bulunmuştur. Bunlardan 32 hastaya ait 51 �rnekte viral y�k kantitasyon alt sınırından daha d�ş�kt�r. On sekiz hastaya ait 27 (%12.5) �rnekte viral y�k ortalama 802 kopya/ml (aralık: 80-8369 kopya/ml) olarak belirlenmiştir. Antijenemi pozitif olup PCR ile negatif bulunan �rnek yoktur.�
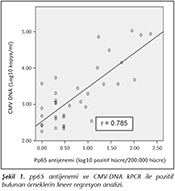
Her iki test ile pozitif saptanan �rnekler değerlendirildiğinde; plazma CMV-DNA kopya/ml sayısı ile pp65 pozitif h�cre sayısı arasındaki korelasyon istatistiksel olarak anlamlı bulunmuştur (r= 0.785). Lineer regresyon analizi Şekil 1'de g�sterilmiştir.
CMV antijenemi ve CMV PCR testleri farklı g�nlerde �alışılan 31 �rnek �ifti bulunmaktadır. Bunlardan beşi, hasta tedavi almakta iken �alışılmıştır. Bu olgulardan birinde her iki test negatif, birinde her iki test pozitif, ���nde ise antijenemi negatif ancak CMV-DNA PCR pozitif bulunmuştur. Antijenemi ve PCR testlerindeki viral kinetikler tedavi altında farklı olabildiği i�in, s�z konusu beş �rnek �ifti ROC analizine dahil edilmemiştir.
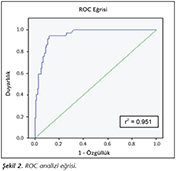
Antijenemi pozitifliğine karşılık gelen CMV-DNA değerini belirlemek amacıyla, pp65 antijenemi pozitifliği (≥ 1 pozitif h�cre/200.000 h�cre) esas alınarak ROC analizi yapılmıştır (Şekil 2). Antijenemi pozitifliğine karşılık gelen CMV-DNA d�zeyi, %91.7 duyarlılık ve %90.3 �zg�ll�k ile 205 kopya/ml olarak belirlenmiş; ROC analizine ilişkin sonu�lar Tablo III'te g�sterilmiştir. Antijenemi negatif ancak viral y�k� 205 kopya/ml'nin �zerinde olan 17 �rnek �ifti bulunmuştur. Bu �rnekler antijenemi negatif/PCR pozitif toplam 75 �rneğin %22.6'sını oluşturmaktadır.
Antijenemi testinin pozitifliği esas alındığında, CMV-DNA kPCR testinin duyarlılığı %100, �zg�ll�ğ� %56.6, PPD %32.2 ve NPD %100 olarak saptanmıştır.
TARTIŞMA
Gerek testler arası değişkenler, gerekse hastalarda kullanılan tanı, izlem ve tedavi farklılıkları, solid organ transplant (SOT) alıcılarında CMV enfeksiyonu i�in klinik kararlarda kullanılacak viral eşik değerler konusunda fikir birliği oluşmasını g��leştirmektedir. D�nya Sağlık �rg�t� tarafından 2010'da CMV-DNA uluslararası standardının (IS) geliştirilmesi, testler arası değişkenliklerin azaltılması i�in �nemli bir basamak olmuştur. Ancak halen her merkezin kendi koşullarına uygun eşik değerleri belirlemesi ve hasta izleminde test değişikliği yapılmaması �nerilmektedir. Merkezimizde SOT alıcılarında, CMV pp65 antijenemi ve plazmada CMV-DNA kPCR sonu�ları karşılaştırılarak, iki test arasındaki korelasyon ile d�ş�k viral y�k d�zeylerinin antijenemi testindeki karşılığı araştırılmıştır. �alışmamızda viremiyi saptamada plazma CMV-DNA PCR ile antijenemi arasındaki uyum %64 olarak bulunmuştur. Uyumsuz �rneklerin t�m� (n= 78) PCR pozitif, antijenemi negatiftir. Bu durum, PCR y�nteminin pp65 antijenemi testine g�re daha duyarlı olmasına bağlıdır1. Antijenemi negatif �rneklerin yarısından fazlasında (%65) viral y�k d�ş�k olup,� kantitasyon alt sınırı olan 80 kopya/ml'nin altındadır.
�alışmamızda, her iki testle pozitiflik saptanan �rneklerin kantitatif sonu�ları arasında iyi bir korelasyon saptanmıştır (r= 0.785). İtalya'dan bildirilen 45 SOT (kalp ve b�brek) alıcısının değerlendirildiği bir �alışmada, pozitif antijenemi ve pozitif CMV-DNA viral y�k değerleri arasındaki korelasyon benzer (r= 0.718) olarak saptanmıştır1. �alışmamızda 53 �rnekte (%24.4) viral y�k, testin kantitasyon alt sınırının altında sonu�lanmıştır, bu değerleri klinik a�ıdan yorumlamak zordur. CMV-DNA kPCR testinin duyarlılık, �zg�ll�k ve prediktif değerleri incelendiğinde; enfeksiyonu ekarte etmede başarılı olduğu (%100 NPD), ancak pozitif saptandığında antijenemi pozitifliğine kanıt olamayacağı g�r�lmektedir (%32.2 PPD).
�alışmamızda pp65 antijenemi pozitifliği (≥1 pozitif h�cre/200.000 h�cre) esas alınarak uygulanan ROC analizinde; SOT alıcılarında antijenemi pozitifliğine denk gelen CMV-DNA eşik değeri, 205 kopya/ml (duyarlılık: %91.7, �zg�ll�k: %90.3) olarak bulunmuştur. Bu sonu�, merkezimizde kullanılan testler ve �alışmanın yapıldığı hasta pop�lasyonu i�in, kPCR y�ntemiyle pozitiflik saptandığında, hangi d�zeylerin daha anlamlı olabileceği konusunda klinisyenlere yol g�stermektedir. Buna g�re, 205 kopya/ml altındaki viral y�k sonu�larında belirlenen g�ven aralığında, antijenemi testinin negatif olacağı �ng�r�lerek karar verilebilir. Benzer bir �alışma, T�rkiye'de k�k h�cre transplantasyonu alıcılarında yapılmış, CMV pp65 antijenemi testi ile iki farklı kPCR testi sonu�ları karşılaştırılmıştır7. Bu �alışmada, antijenemi pozitifliğine (≥ 1 pozitif h�cre/ 200.000 h�cre) karşılık gelen viremi değeri testlerden birinde 1543.5 kopya/ml, diğerinde 423 kopya/ml olarak belirlenmiştir7.�
Sunulan bu �alışma, hasta izlem sonu�larını ve klinik verileri kapsamamaktadır. Bu nedenle SOT alıcılarında CMV ile ilişkili hastalıkların preemptif tedavi ile �nlenmesi ve tanısı i�in klinik a�ıdan anlamlı eşik değerlere duyulan gereksinime tam olarak yanıt vermemektedir. Genel olarak, antijenemi testi CMV hastalığından 5-14 g�n �nce, PCR ise antijenemiden yaklaşık bir hafta �nce pozitifleşmektedir. Yapılan bir �alışmada, b�brek transplantasyonunda seropozitif alıcı ve verici �ifti i�in preemptif tedavi başlama sınır değeri olarak antijenemi testinde 4 pozitif h�cre/1.000.000 h�cre, laboratuvar yapımı kPCR testinde 2.000 kopya/ml sınırının kullanılması �ng�r�lm�şt�r8. SOT alıcılarında gerek antijenemi gerekse CMV-DNA PCR sonu�ları; alıcı ve vericinin CMV a�ısından seropozitifliği, alıcının imm�n s�presyonu, uygulanan tedavi, antiviral profilaksi verilip verilmemesi, kullanılan testlerin �zellikleri gibi bir�ok parametreden etkilenmektedir6. Kemik iliği transplant alıcılarında ise, viral dinamiklerin daha hızlı olduğu ve d�ş�k viral y�k�n bile klinik a�ıdan anlamlı olduğu g�sterilmiştir2,4.
CMV pp65 antijenemi ile CMV-DNA PCR testleri arasında genel bir uyum olmakla birlikte, testlerin farklı parametreleri değerlendirdiği g�z �n�ne alınmalıdır. Uyumsuz test sonu�ları değerlendirilirken, PCR'nin genellikle antijenemiden �nce pozitifleştiği, tedavi alan hastalarda ilk g�nlerde PCR testinde viral y�kte bir artış saptanabileceği, ileri l�kopeni durumlarında antijenemi testinin negatif olabileceği hatırlanmalıdır9,10.��
CMV seroloji sonu�ları ile viremi arasında doğrudan bir ilişki bulunmamaktadır. Bu nedenle, SOT alıcılarında CMV enfeksiyonunu değerlendirmede serolojik g�stergelerin yeri sınırlı olup, transplantasyon �ncesi alıcı ve vericide seropozitifliğin belirlenmesine y�neliktir. CMV IgM ve IgG birlikte pozitif bulunan tek olgumuzda, viremi değerlendirmesi tek �rnekte yapılmış, antijenemi ve CMV-DNA testleri negatif bulunmuştur.
Sonu� olarak bu �alışmada, karaciğer ve b�brek transplant alıcılarından oluşan bir grupta pp65 antijenemi testinde 1 pozitif h�cre/200.000 h�creye karşılık gelen CMV-DNA PCR testi değeri 205 kopya/ml olarak belirlenmiştir. Bu sonu�, hasta izleminde testler arasında ge�iş yapıldığında ve d�ş�k viral y�k sonu�larının klinik a�ıdan yorumlanmasında yardımcı olacaktır.
TEŞEKK�R
Dr. Erdem Erkoyun ve Dr. Yasin Sağlam'a istatistiksel analizlerdeki katkılarından dolayı teşekk�r ederiz.
KAYNAKLAR
- Boarettia M, Sorrentino A, Zantedeschi C, Forni A, Boschiero L, Fontana R. Quantification of cytomegalovirus DNA by a fully automated real-time PCR for early diagnosis and monitoring of active viral infection in solid organ transplant recipients. J Clin Virology 2012; 56(2): 124-8.
- Waggoner J, Ho DY, Libiran P, Pinsky BA. Clinical significance of low cytomegalovirus DNA levels in human plasma. J Clin Microbiol 2012; 50(7): 2378-83.
- Allice T, Cerutti F, Pittaluga F, et al. Evaluation of a novel real-time PCR system for cytomegalovirus DNA quantitation on whole blood and correlation with pp65 test in guiding pre-emptive antiviral treatment. J Virol Methods 2008; 148(1-2): 9-16.
- Kalpoe JS, Kroes AC, de Jong MD, et al. Validation of clinical application of cytomegalovirus plasma DNA load measurement and definition of treatment criteria by analysis of correlation to antigen detection. J Clin Microbiol 2004; 42(4): 1498-504.
- Pang XL, Fox JD, Fenton JM, et al. Interlaboratory comparison of cytomegalovirus viral load assays. Am J Transplant 2009; 9(2): 258-68.
- Razonable RR, Hayden RT. Clinical utility of viral load in management of cytomegalovirus infection after solid organ transplantation. Clin Microbiol Rev 2013; 26(4): 703-27.
- �olak D, Kazık M, Mutlu D, Uygun V, Karag�l A, Hazar V. Assesment of cytomegalovirus (CMV) load in hematopoietic stem cell transplant recipients by CMV antigenemia and two different real-time PCR assays. J Clin Virol 2009; 46 (Suppl 1): S47.
- David-Neto E, Triboni AH, Paula FJ, et al. A double-blinded, prospective study to define antigenemia and quantitative real-time polymerase chain reaction cutoffs to start preemptive therapy in low-risk, seropositive, renal transplanted recipients. Transplantation 2014; 98(10): 1077-81.
- Rhee JY, Peck KR, Lee NY, Song JH. Clinical usefulness of plasma quantitative polymerase chain reaction assay: diagnosis of cytomegalovirus infection in kidney transplant recipients. Transplant Proc 2011; 43(7): 2624-9.
- Kraft CS, Armstrong WS, Caliendo AM. Interpreting quantitative cytomegalovirus DNA testing: understanding the laboratory perspective. Clin Infect Dis 2012; 54(12): 1793-7.
İletişim (Correspondence):
Prof. Dr. A. Arzu Sayıner,
Dokuz Eyl�l �niversitesi Tıp Fak�ltesi,
Tıbbi Mikrobiyoloji Anabilim Dalı,
Bal�ova, İzmir, T�rkiye.
Tel (Phone): +90 232 412 4501,
E-posta (E-mail): arzu.sayiner@deu.edu.tr