Yüksek
Risk Altındaki Hastaların Klinik Örneklerinde BK ve JC Virus DNA Pozitifliğinin
Gerçek Zamanlı Polimeraz Zincir Reaksiyonu ile Araştırılması*
Investigation
of BK and JC Virus DNA Positivities by Real-Time Polymerase Chain Reaction in
the
Clinical Samples of Patients with High Risk
Seyyal
ROTA1, Kibriya FİDAN2, Gülendam BOZDAYI1,
Aydın DALGIÇ3, Işıl FİDAN1, Gülsan SUCAK4,
Tuba MÜDERRİS1
1 Gazi Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Ankara.
1 Gazi University Faculty of Medicine, Department of Medical Microbiology, Ankara, Turkey.
2 Gazi Üniversitesi Tıp Fakültesi, Çocuk Sağlığı ve Hastalıkları Anabilim Dalı, Ankara.
2 Gazi University Faculty of Medicine, Department of Pediatrics, Ankara, Turkey.
3 Gazi Üniversitesi Tıp Fakültesi, Genel Cerrahi Anabilim Dalı, Ankara.
3 Gazi University Faculty of Medicine, Department of General Surgery, Ankara, Turkey.
4 Gazi Üniversitesi Tıp Fakültesi, Kemik İliği Transplantasyon Ünitesi, Ankara.
4 Gazi University Faculty of Medicine, Department of Bone Marrow Transplantation Unit, Ankara, Turkey.
* Bu çalışma XXXIII. Türk Mikrobiyoloji Kongresi (21-25 Ekim 2008, Bodrum) ve XII. Annual ESCV Meeting (27-30 Eylül 2009, İstanbul)’de sunulmuştur.
ÖZET
İnsan polyomavirusları olan BK virus (BKV) ve JC virus (JCV), toplumlarda yaygın olarak bulunan ve latent enfeksiyon oluşturan küçük DNA viruslarıdır. Hayatın erken dönemlerinde kazanılan primer BKV/JCV enfeksiyonları genellikle asemptomatik seyretmektedir. Ancak kemik iliği ve solid organ transplantasyonu yapılan ya da kanserli hastalar gibi immün sistemi baskılanmış hastalarda bu virusların reaktivasyonu ciddi klinik tablolara yol açabilmektedir. Bu retrospektif çalışmanın amacı, polyomavirus enfeksiyonu yönünden yüksek risk altındaki hastaların klinik örneklerinde BKV ve JCV DNA varlığının gerçek zamanlı polimeraz zincir reaksiyonu (RT-PCR) ile araştırılmasıdır. Çalışmaya, Temmuz 2007-Ocak 2009 tarihleri arasında, immün sistemi bozuk/baskılanmış hastaların yattığı kliniklerden laboratuvarımıza gönderilen, 115 hastaya ait toplam 268 örnek (62 kan, 206 idrar) dahil edilmiştir. İdrar ve kan örneklerinden viral nükleik asit izolasyonu “High Pure PCR Template Preparation Kit” (Roche, Almanya) ile yapılmış ve DNA’lar küçük t antijeninin 174 (JCV) ve 219 (BKV) baz çiftlik bölgesini çoğaltan primer dizilerini içeren amplifikasyon karışımı (TIB Molbiol GmbH, Almanya) ve hibridizasyon probları (Roche, Almanya) kullanılarak LightCycler (Roche Applied Science, Almanya) cihazı ile çoğaltılmıştır. Çalışmaya alınan örneklerde polyomavirus DNA pozitifliği %33.2 (89/268) olarak saptanmıştır. BKV ve JCV DNA pozitifliği örneklere göre değerlendirildiğinde; idrar örneklerinin %25.2 (53/206)’sinde BKV, %14.5 (30/206)’inde JCV ve %2.4 (5/206)’ünde hem BKV hem de JCV DNA varlığı tespit edilmiştir. Kan örneklerinin sadece birinde (1/62; %1.6) BKV DNA pozitifliği belirlenirken, hiçbirisinde JCV DNA’sı saptanmamıştır. Örneklerdeki BKV ve JCV DNA pozitiflik oranlarının gönderildikleri kliniklere göre dağılımı ise sırasıyla; çocuk nefroloji servisi için %24.3 ve %9.5; böbrek transplantasyon ünitesi için %9.6 ve %8.2; erişkin nefroloji servisi için %13.5 ve %18.9; kemik iliği transplantasyon ünitesi için %30.8 ve %15.4; çocuk hastalıkları kliniği için %22.9 ve %8.6 olarak saptanmıştır. Çocuk hematoloji servisinden gelen örneklerde %36.4 oranında (4/11) BKV pozitifliği saptanmasına karşın JCV pozitifliği izlenmemiş; erişkin hematoloji servisinden gelen üç örneğin birinde JCV pozitifliği saptanmasına karşın BKV pozitifliği bulunmamıştır. Yoğun bakım ünitesinden gelen altı örneğin üçünde BKV saptanırken, çocuk endokrinoloji servisinden gelen iki örnekte de JCV saptanmıştır. BK viremisinin tespit edildiği tek hasta böbrek transplantasyon ünitesinde yatmaktadır. Her iki virusa ait DNA pozitifliği idrar örneklerinde %1.9 (5/268) gibi oldukça düşük oranda saptanmıştır. Çalışılan örneklerin %24.7 (22/89)’sinde BKV DNA ≥ 107 kopya/ml, %2.2 (2/89)’sinde JCV DNA ≥ 107 kopya/ml, %2.2 (2/89)’sinde ise hem BKV hem de JCV DNA’ları ≥ 107 kopya/ml olarak belirlenmiş; bu örneklerin tümünün idrar olduğu izlenmiştir. Bu çalışmadan elde edilen veriler, hastanemizde immünsüpresif hastaların izlendiği klinikler ile BKV/JCV enfeksiyonlarının tanısı ve hastaların takibi konusunda ortak bir algoritma belirlenmesine olanak sağlamıştır. Sonuç olarak, BKV ve JCV reaktivasyon ve enfeksiyonlarının önem taşıdığı hasta gruplarında özellikle de kemik iliği ve böbrek nakli yapılan merkezlerde, tanı ve takibe yönelik programların oluşturulması gerektiği düşünülmüştür.
Anahtar sözcükler: BK virusu; JC virusu; gerçek zamanlı polimeraz zincir reaksiyonu; transplantasyon; immünsüpresif hasta.
ABSTRACT
Human polyomaviruses, namely BK (BKV) and JC (JCV) viruses are small DNA viruses that cause latent infections worldwide. Primary infections are usually acquired in the early periods of life and are generally asymptomatic. However BKV/JCV infections may cause severe clinical conditions in immunosuppressive patients such as bone marrow and solid organ transplantation or cancer patients. The aim of this retrospective study was to investigate the presence of BKV and JCV nucleic acids by real-time polymerase chain reaction (RT-PCR) in the clinical samples of patients with high risk. A total of 268 (62 blood, 206 urine) samples obtained from 115 immunocompromised patients hospitalized in Gazi University Hospital between July 2007 to January 2009, were included to the study. Viral nucleic acids were extracted from the samples with High Pure PCR Template Preparation Kit (Roche, Germany). By using amplification mix (TIB Molbiol GmbH, Germany) that included primers targeting 174 (JCV) and 219 (BKV) base pair fragments of the small t antigen, and hybridization probes (Roche, Germany), nucleic acids were amplified with LightCycler (Roche Applied Science, Germany) system. As a result, total polyomavirus DNA positivity rate was found as 33.2% (89/268). When BKV and JCV DNA positivities were evaluated according to the samples, 25.2% (53/206) of urine samples yielded positive results for BKV, 14.5% (30/206) for JCV and 2.4% (5/206) for both BKV and JCV. Only one of the blood samples (1/62; 1.6%) were found positive by means of BKV DNA, while none of the blood samples were positive for JCV DNA. The distribution of BKV and JCV DNA positivity rates according to the inpatient clinics were as follows, respectively; 24.3% and 9.5% for pediatric nephrology, 9.6% and 8.2% for renal transplantation unit, 13.5% and 18.9% for adult nephrology, 30.8% and 15.4% for bone marrow transplantation unit, 22.9% and 8.6% for pediatric clinics. In samples from pediatric hematology patients, BKV positivity was 36.4% (4/11), while there were no JCV positivity. However, in hematology patients, while JCV was positive in one of the three samples, no BKV positivity was detected. BKV was seen in three of six samples obtained from patients in the intensive care unit. JCV was positive in both of the two samples obtained from patients in pediatric endocrinology. The only patient that had BKV DNA in blood sample was a renal transplant patient. BKV + JCV DNAs were positive together in only five (1.9%) of the urine samples. In 24% (22/89) of the samples, BKV DNA was found ≥ 107 copies/ml, in 2.2% (2/89) JCV DNA was ≥ 107 copies/ml, whereas in 2.2% (2/89) of samples both BKV and JCV DNA was ≥ 107 copies/ml. All of those samples with high DNA levels were urine. The data of this study led to the establishment of a collaborative algorithm between the laboratory and clinics in our hospital for the diagnosis and follow-up of the patients in terms of BKV/JCV infections. In conclusion, since BKV/JCV reactivations and infections are crutial in immunosuppressive patients, especially medical centers specialized in bone marrow and renal transplantation, diagnostic and monitoring procedures related to those infections should be programmed.
Key words: BK virus; JC virus; real-time polimerase chain reaction; transplantation; immunosuppressive patient.
Geliş Tarihi (Received): 09.07.2010 • Kabul Ediliş Tarihi (Accepted): 07.02.2011
GİRİŞ
Polyomaviridae ailesinde sınıflandırılan BK ve JC virusları (sırasıyla; BKV ve JCV), küçük, zarfsız, ikozahedral yapılı, çift iplikli DNA viruslarıdır1. İlk kez 1971 yılında tanımlanan bu viruslar izole edildikleri hastaların ad ve soyadlarının baş harfleri ile isimlendirilmişlerdir2. BK ve JC virusları, DNA düzeyinde %75, aminoasit düzeyinde ise %68 homoloji göstermektedir1. Her iki virus da, hayatın ilk 10-15. yılında kazanılmakta ve enfeksiyonlar genellikle asemptomatik geçirilmektedir2. Polyomaviruslar toplumlarda yaygın olarak bulunmakta olup, BKV ve JCV seropozitifliği yaşa ve bölgelere göre değişiklik göstermektedir2. Genel olarak BKV seroprevalansının 5-9 yaşlarında %70-90’a ulaştığı, JCV seroprevalansının ise 25 yaşından sonra %50-72 arasında değiştiği belirtilmektedir2,3. Ülkemizde, 1123 sağlıklı kişinin dahil edildiği bir çalışmada, BKV seroprevalansı %78.5 olarak saptanmış ve seropozitifliğin 1-10 yaş grubunda, > 10 yaş gruba oranla daha yüksek olduğu bildirilmiştir4. Bu sonuç ülkemizde de BKV enfeksiyonlarının yaygın olduğunu ve virusun çocukluk döneminde kazanıldığını vurgulamaktadır.
Primer enfeksiyonu takiben, BKV, ürogenital kanal, böbrek ve santral sinir sistemini de içeren çeşitli dokularda, JCV ise B lenfositlerinde latent olarak kalmaktadır1,5,6. Bu viruslar, immün sistemin baskılanması sonucu reaktive olarak litik enfeksiyon oluşturur ve çeşitli klinik bulguların ortaya çıkmasına yol açabilir1,7. Spontan BKV reaktivasyonu, sağlıklı bireylerin %5-20’sinde görülebilmekte ve düşük düzeyde replikasyon ile idrarda virus atılımı olabilmektedir. BKV reaktivasyonunun asemptomatik hematüri, hemorajik sistit, nefrit, üreter ülserasyonu veya darlığına neden olabildiği; allograft alıcılarında ise graft atılımı ve nefropatiye yol açabildiği bilinmektedir3,5,8. İmmünkompromize hastalarda JCV reaktivasyonu ise, virusun santral sinir sisteminde oligodendrositleri etkilemesi sonucu progresif multifokal lökoensefalopati (PMLE) gelişimine yol açabilir1,8.
BKV ve JCV reaktivasyonları, immünsüpresif tedavi alan böbrek ve kemik iliği transplantlı hastalar ile kanserli hastalar için ciddi klinik öneme sahiptir8. Dolayısıyla bu hastalarda enfeksiyonların erken tanısı, immünsüpresif ilaç dozunun azaltılması ve/veya alternatif ilaç tedavilerinin planlanması açısından değerlidir.
Bu retrospektif çalışmada, polyomavirus enfeksiyonu yönünden yüksek risk altındaki hastaların klinik örneklerinde BKV ve JCV DNA varlığının gerçek zamanlı polimeraz zincir reaksiyonu (RT-PCR) ile araştırılması amaçlanmıştır.
GEREÇ ve YÖNTEM
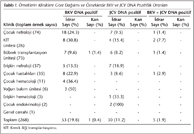
Çalışmaya, Temmuz 2007-Ocak 2009 tarihleri arasında, immün sistemi bozuk/baskılanmış hastaların yattığı kliniklerden (transplantasyon üniteleri, nefroloji, hematoloji, yoğun bakım vb.) laboratuvarımıza gönderilen, 115 hastaya ait toplam 268 örnek (62 kan, 206 idrar) dahil edildi (Tablo I). Örneklerden BKV ve JCV nükleik asitlerinin ekstraksiyonu, “High Pure PCR Template Preparation” kiti (Roche, Almanya) ile üreticinin önerileri doğrultusunda yapıldı.
İdrar ve kan örneklerinden elde edilen DNA’lar; küçük t antijenin “A” 174 baz çift (bç)’lik parçası (polyomavirus JC) ve “a” 219 bç’lik parçasını (polyomavirus BK) çoğaltan primer dizilerini içeren “Light Mix” (TIB Molbiol GmbH, Almanya) amplifikasyon karışımı ve “Light Cycler Fast Start DNA Master Hybridization” probları (Roche, Almanya) kullanılarak LightCycler-1.5 (Roche Applied Science, Almanya) cihazı ile çoğaltıldı. Ürünlerin erime eğrisi ve erime noktası (Tm) analizleri yine aynı cihazda yapıldı. BKV pozitif örnekler kanal 640’ta 64 ± 2°C’de pik veren BKV standartları ile birlikte; JCV pozitif örnekler kanal 705’te 68 ± 2°C’de pik veren JCV standartları ile birlikte değerlendirildi. Her iki virus için de kullanılan negatif kontrollerde herhangi bir pik gözlenmedi. Her çalışmada, sayısal değerin hesaplanabilmesi için altı adet BKV standart, altı adet JCV standart, bir adet negatif kontrol çalışmaya dahil edildi. Alınan negatif sonuçların geçerliliği, çalışmaya konulan internal kontrol ile denetlendi. Kullanılan kitin saptama alt sınırı 10 kopya/ml; üst sınırı ise plazma için 7000 kopya/ml, idrar için 15.000 kopya/ml olup, üretici firma tarafından kitin duyarlılığı %97.2, özgüllüğü ise %100 olarak verilmekte idi.
İstatistiksel değerlendirmede ki-kare testi kullanıldı ve analizler SPSS for Windows version 15.0 (Chicago, ABD) ile yapıldı. p< 0.05 değeri anlamlı kabul edildi.
BULGULAR
Çalışmaya alınan 115 hastaya ait 268 örneğin 89 (%33.2)’unda, BKV ve/veya JCV DNA varlığı saptanmıştır. Örneklerin gönderildiği kliniklere göre dağılımı ile BKV ve JCV DNA pozitiflik oranları Tablo I’de görülmektedir. Toplu olarak değerlendirildiğinde; 206 idrar örneğinin 53 (%25.7)’ünde BKV DNA, 30 (%14.5)’unda JCV DNA, 5 (%2.4)’inde ise hem BKV hem de JCV DNA’sı pozitif olarak saptanmıştır. Kan örneklerinin sadece birinde (1/62; %1.6) BKV DNA pozitifliği belirlenirken, hiçbirisinde JCV DNA’sı tespit edilmemiştir (Tablo I).
BKV DNA ve JCV DNA pozitiflik oranlarının, örneklerin gönderildiği kliniklere göre dağılımında istatistiksel olarak anlamlı bir fark belirlenmemiştir (sırasıyla; p= 0.055 ve p= 0.478).
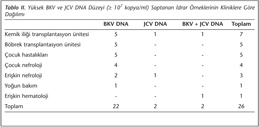
Viral nükleik asit pozitifliği saptanan 89 örneğin 26 (%29.2)’sında kantitatif DNA düzeylerinin ≥ 107 kopya/ml olduğu tespit edilmiş ve hepsi idrar olan bu örneklerin kliniklere göre dağılımı Tablo II’de verilmiştir.
TARTIŞMA
Hayatın erken dönemlerinde kazanılan ve vücutta latent olarak kalan BKV ve JCV, özellikle düşkün ya da bağışıklık sistemi bozuk veya baskılanmış kişilerde reaktive olarak ciddi klinik tablolara neden olabilir7,8. Bu çalışmada, BKV ve JCV reaktivasyon riski yüksek olan hastaların klinik örneklerinde viral nükleik asit varlığı RT-PCR yöntemiyle araştırılmış ve pozitifliğin saptandığı örneklerin kliniklere göre dağılımı belirlenmiştir. Çalışılan örneklerde toplam BKV ve/veya JCV DNA pozitiflik oranı %33.2 (89/268) olarak bulunmuş ve en yüksek pozitiflik oranının (14/26; %53.8), beklenildiği gibi, kemik iliği transplantasyon ünitesinden gelen örneklere ait olduğu izlenmiştir. Bu oran çocuk hematoloji, çocuk nefroloji, çocuk hastalıkları, erişkin nefroloji ve böbrek transplantasyon ünitesinden gelen örnekler için sırasıyla %36.4 (4/11), %35.1 (26/74), %34.3 (12/35), %32.4 (12/37) ve %20.5 (15/73) olarak saptanmıştır.
Kemik iliği transplantasyonu (KİT) yapılan hastalarda 2-8. haftalarda idrarla BKV salınımı olmakta, ancak viruri asemptomatik seyredebilmektedir. Yüksek doz kemoterapi ve KİT uygulanan hastaların %50-80’inde BK virurisi olduğu ve bunların da %64’ünde geç başlangıçlı hemorajik sistit (HS) geliştiği bildirilmektedir9. Erken başlangıçlı HS yüksek doz kemoterapi sonrası ilk 48 saat içerisinde görülürken, geç başlangıçlı HS 48 saatten sonra ortaya çıkar ve en sık rastlanan etkenler BKV ve adenoviruslardır10. Bizim çalışmamızda KİT hastalarının idrar örneklerinde saptanan BKV DNA pozitifliği (10/26), bu hastaların klinik seyirlerinin izlenmesi gereğini ortaya koymaktadır.
Böbrek transplantasyonu (BT) sonrası takip edilen hastalarda BKV pozitiflik oranının JCV’den daha yüksek olduğu bildirilmektedir5,7,11. Saundh ve arkadaşları7, BT yapılan 30 hastayı izledikleri çalışmalarında, sekiz hastada BK virurisi saptamışlar ve 12 ay sonra bunların sadece birinde biyopsi ile doğrulanan nefropati geliştiğini, JC virurisi saptadıkları beş hastada ise nefropati oluşmadığını bildirmişlerdir. Bu araştırıcılar, BKV reaktivasyonunun transplantasyon sonrası üçüncü ayda gerçekleşirken JC virurisinin daha erken olduğunu belirtmişler; nefropati gelişiminin yüksek düzey (≥ 107 kopya/ml) viruri ile ilişkili olduğunu ve RT-PCR yönteminin BT hastalarında polyomavirus enfeksiyonlarının takibinde kullanılabileceğini ifade etmişlerdir7. Amerikan Transplantasyon Derneği, BT hastalarında polyomavirus DNA’sının idrarda ≥ 107 kopya/ml, plazmada ise ≥ 104 kopya/ml olması halinde klinik olarak nefropatinin gelişebileceğini kabul etmektedir12. Bizim çalışmamızda da, kantitatif değerlendirme bu veriye göre yapılmış ve BKV/JCV pozitif idrar örneklerinin %29.2 (26/89)’sinde DNA düzeylerinin ≥ 107 kopya/ml olduğu saptanmıştır (Tablo II). Bu durum, viruri düzeyinin yüksek olduğu bu hastaların ileriki dönemlerde nefropati gelişimi açısından risk altında olduğunu düşündürmektedir. Ancak örneklerin alındığı hastaların klinik bilgilerine ulaşılamamış ve klinik ve laboratuvar izlemlerinin yapılamamış olması, çalışmamızın en önemli sınırlamasıdır.
Costa ve arkadaşları5, BT yapılan 109 hastadan aldıkları 138 renal ve üretral doku örneğinde RT-PCR yöntemiyle yaptıkları çalışmada, BKV DNA pozitifliğini %29.6, JCV DNA pozitifliğini ise %18.3 oranında bulmuşlar ve renal allograft biyopsilerinde viral DNA kantitasyonunun nefropati gelişiminde yol gösterici olabileceğini bildirmişlerdir. Kaneko ve arkadaşlarının13 çalışmasında ise, 45 böbrek alıcısı hastaya ait idrar örneklerinde RT-PCR ile BKV ve JCV DNA pozitifliğinin aynı oranda (%33.3) olduğu bulunmuştur. Ülkemizde de, BT’den sonra BKV reaktivasyonları ile ilgili raporlar mevcuttur14,15,16,17,18,19. 1992 yılında Us ve Ustaçelebi14, böbrek ve kemik iliği transplantasyonu yapılan 10 hastanın dördünde BKV reaktivasyonunu serolojik olarak göstermişlerdir. Senger ve arkadaşları16 da, BT yapılmış 18 hastadan birinde RT-PCR BKV viremisi saptamışlar ve immünsüpresif tedavi dozunun azaltılmasıyla BKV yükünün azaldığını bildirmişlerdir. Yazısız ve arkadaşlarının17 yaptığı çalışmada, kemik iliği ve kök hücre nakli yapılan 12 hasta izlenmiş ve tümünde RT-PCR ile bir veya birden fazla idrar ve kan örneğinde BKV pozitifliği saptanmıştır. Hemorajik sistit gelişen iki hastadan bir tanesi BKV ile ilişkilendirilmiş ve immünsüpresyon dozu azaltılarak klinik düzelme sağlanmıştır17. Fidan ve arkadaşları18 ise, BT yapılan ancak BKV enfeksiyonu gelişimi nedeniyle graft reddinin ortaya çıktığı iki çocuk olguyu rapor etmişlerdir. Bu araştırıcılar, transplantasyon sonrası görülen BKV nefropatisi riskinin belirlenmesinde, kan ve idrarda viral yük tayini ve izleminin önem taşıdığını vurgulamışlardır18.
Bizim çalışmamızda, BT ünitesinde yatan hastalar ile BT yapıldıktan sonra çocuk/erişkin nefroloji kliniklerinde takip edilen hastalara ait örnekler toplu olarak değerlendirildiğinde, idrarda BKV DNA pozitifliği %17.4 (32/184) ve JCV DNA pozitifliği %11.9 (22/184) olarak belirlenmiş; buna karşın sadece bir kan örneğinde (1/184; %0.5) BKV DNA pozitif olarak saptanmıştır. BK viremisi tespit edilen bu tek hastanın (1/115; %0.9) BT ünitesinde yatan bir hasta olduğu izlenmiştir. Sonuçlarımız, BT yapılan hastalarda BKV reaktivasyonlarının JCV’den daha yüksek olduğu verisini desteklemektedir. Her ne kadar saptadığımız BKV/JCV DNA pozitifliklerinin reaktivasyon sonucu olduğu düşünülmüşse de, hastaların transplantasyon öncesi seropozitiflik durumları bilinmediğinden bu konuda net bir sonuca varmak mümkün değildir.
BK ve JC viruslarının, gerek seronegatif bir alıcıya seropozitif bir vericinin dokusu ile nakledilerek, gerekse önceden seropozitif alıcılarda immünsüpresif ilaçların kullanımı ile reaktive olarak, immün sistemi baskılanmış hastalarda ciddi klinik tablolara neden olabileceği iyi bilinmektedir20. Dolayısıyla özellikle kemik iliği ve BT yapılan merkezlerde, BKV ve JCV enfeksiyonlarının erken ve doğru tanısı için uygun yöntemlerin kullanılması ve takibe yönelik bir algoritmanın oluşturulması gerekmektedir. Nitekim bu çalışmadan elde edilen veriler ile, hastanemizde riskli hasta gruplarının yattığı klinikler ile BKV ve JCV enfeksiyonlarının tanısı ve hastaların takibi konusunda ortak bir algoritma belirlenmiştir. Buna göre; BT yapılacak hastalardan nakil öncesi ve nakil sonrası 7. gün, 1. ay, 3. ay, 6. ay ve 12. aylarda olmak üzere alınacak örneklerde BKV ve JCV DNA’larının PCR ile araştırılmasına; ayrıca kök hücre nakli yapılan ve takiplerinde hematüri görülen hastalardan idrar sitolojisi ve idrar kültürü incelemelerinin yanı sıra idrarda BKV/JCV PCR analizi yapılmasına ve pozitif sonuç alınan (klinikte bu durumu açıklayacak başka bir patolojik bulgu saptanmayan) hastalara tedavi başlanarak viral yükün kantitatif olarak izlenmesine karar verilmiştir.
KAYNAKLAR
- Vilchez RA, Kusne S. Molecular and clinical perspectives of polyomaviruses: emerging evidence of importance in non-kidney transplant populations. Liver Transpl 2006; 12(10): 1457-63. [Özet]
- Knowles WA. Discovery and epidemiology of the human polyomaviruses BK virus (BKV) and JC virus (JCV). Adv Exp Med Biol 2006; 577(1): 19-45. [Özet]
- Ribeiro T, Fleury MJ, Granieri E, et al. Investigation of the prevalence of antibodies against neurotropic polyomaviruses BK, JC and SV40 in sera from patients affected by multiple sclerosis. Neurol Sci 2010; 31: 517-21. [Özet]
- Us D, Hayran M, Ustacelebi S. New human polyomavirus; BK virus antibody levels in different age groups using the hemagglutination inhibition test. Mikrobiyol Bul 1991; 25(2): 173-7. [Özet]
- Costa C, Bergallo M, Sidoti F, et al. Polyomaviruses BK- and JC-DNA quantitation in kidney allograft biopsies. J Clin Virol 2009; 44(1): 20-3. [Özet]
- Comar M, Zanotta N, Bovenzi M, Campello C. JCV/BKV and SV40 viral load in lymphoid tissues of young immunocompetent children from an area of north-east Italy. J Med Virol 2010; 82(7): 1236-40. [Özet]
- Saundh BK, Tibble S, Baker R, Sasnauskas K, Harris M, Hale A. Different patterns of BK and JC polyomavirus reactivation following renal transplantation. J Clin Pathol 2010; 63(8): 714-8. [Özet]
- Boothpur R, Brennan DC. Human polyoma viruses and disease with emphasis on clinical BK and JC. J Clin Virol 2010; 47(4): 306-12. [Özet]
- Güneş D, Uysal KM. Yüksek doz kemoterapi ve hematopoietik kök hücre transplantasyonu uygulanan çocuklarda hemorajik sistit. UHOD-Uluslararası Hematoloji Onkoloji Dergisi 2007; 17(2): 118-28. [Özet] [PDF]
- Kürekçi AE, Atay AA, Azık F, Güney Ç, Erduran E. Allojeneik kemik iliği nakli sonrası polyomavirus hominis tip 1 (BKV)’e bağlı geç başlangıçlı hemorajik sistit. IV. Ulusal Kemik İliği Transplantasyonu ve Kök Hücre Tedavileri Kongresi. 1-4 Mart 2007, Bursa. Kongre Kitabı, S27.
- Randhawa P, Ho A, Shapiro R et al. Correlates of quantitative measurement of BK polyomavirus (BKV) DNA with clinical course of BKV infection in renal transplant patients. J Clin Microbiol 2004; 42: 1176-1180. [Özet] [Tam Metin] [PDF]
- Humar A, Michaels M. American Society of Transplantation recommendations for screening, monitoring and reporting of infectious complications in immunosuppression trials in recipients of organ transplantation. Am J Transplant 2006; 6(2): 262-74. [Özet] [Tam Metin] [PDF]
- Kaneko T, Moriyama T, Tsubakihara Y, Horio M, Imai E. Prevalence of human polyoma virus (BK virus and JC virus) infection in patients with chronic renal disease. Clin Exp Nephrol 2005; 9(2): 132-7. [Özet]
- Us D, Ustacelebi S. Detection of BK virus activation in renal and bone marrow transplantation patients using serological and virological methods. Mikrobiyol Bul 1992; 26(3): 214-23. [Özet]
- Demir E, Liebert UG, Soylemezoglu F, Yalaz K, Kose G, Anlar B. Childhood case of progressive multifocal leukoencephalopathy with improved clinical outcome. J Child Neurol 2005; 20(3): 241-4. [Özet]
- Serin Senger S, Kursun E, Arslan H, Colak T, Haberal M. Renal transplant alıcılarında polyomavirus BK ve JC saptanması. III. Ulusal Viroloji Kongresi. 9-13 Aralık 2007, Uludağ. Kongre Kitabı, s: 227, S10.
- Yazısız H, Uygun V, Mutlu D, Özcan A, Hazar V, Çolak D. Kemik iliği/kök hücre transplantasyonu yapılan çocuklarda BK virüs sürveyansı. III. Ulusal Viroloji Kongresi. 9-13 Aralık 2007, Uludağ. Kongre Kitabı, s: 224, S07.
- Fidan K, Soylemezoglu O, Cakir A, Barit G, Dalgic A, Buyan N. BK virus-associated nephropathy in two pediatric kidney recipients. Transplant Proc 2008; 40(1): 310-2. [Özet]
- Gedizlioglu M, Coban P, Ce P, Sivasli IE. An unusual complication of immunosuppression in myasthenia gravis: progressive multifocal leukoencephalopathy. Neuromuscul Disord 2009; 19(2): 155-7. [Özet]
- Jiang M, Abend JR, Johnson SF, Imperiale MJ. The role of polyomaviruses in human disease. Virology 2009; 384(2): 266-73. [Özet]
İletişim (Correspondence):
Prof. Dr. Seyyal Rota,
Gazi Üniversitesi Tıp Fakültesi,
Tıbbi Mikrobiyoloji Anabilim Dalı,
Beşevler 06500, Ankara, Türkiye.
Tel (Phone): +90 312 202 6998,
E-posta (E-mail): seyyalrota3@hotmail.com