Klinik Örneklerde Mycobacterium tuberculosis Varlığının
Gösterilmesinde
Xpert MTB/RIF Sonuçlarının Değerlendirilmesi
Evaluation of Xpert MTB/RIF Results for the Detection of Mycobacterium tuberculosis in Clinical Samples
İhsan Hakkı ÇİFTÇİ1, Mehtap Hülya ASLAN2, Gülşah AŞIK1
1 Afyonkarahisar Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Afyonkarahisar.
1 Afyonkarahisar University Faculty of Medicine, Department of Medical Microbiology, Afyonkarahisar, Turkey.
2 Nihat Kitapçı Göğüs Hastalıkları ve Göğüs Cerrahisi Hastanesi, Erzurum.
2 Nihat Kitapci Chest Disease and Thoracic Surgery Hospital, Erzurum, Turkey.
ÖZET
Tüberküloz tüm dünyayı tehdit eden temel bir sağlık problemidir. Mycobacterium tuberculosis kompleksin hızlı tanısında nükleik asit amplifikasyon testleri Dünya Sağlık Örgütü (DSÖ) tarafından da önerilen popüler testler halini almıştır. Son zamanlarda kullanıma sunulan Xpert MTB/RIF (Cepheid, ABD) sistemi de, gerçek zamanlı polimeraz zincir reaksiyonu (PCR) mekanizmasına dayanan ticari bir moleküler yöntemdir. Bu bütünleşik sistemde; örneklerin işlenmesi, nükleik asit izolasyonu, amplifikasyon ve rifampisin direnci ile ilişkili bilinen mutasyonların saptanması işlemleri tek bir kartuş içerisinde gerçekleşmekte ve iki saat gibi kısa bir süre içinde sonuç alınabilmektedir. Bu çalışmanın amacı, ön işlem uygulanmamış klinik örneklerde M.tuberculosis varlığının saptanmasında Xpert MTB/RIF sisteminin performansının, Bactec 460TB 12B (BD Diagnostic, ABD), Löwenstein-Jensen (LJ) kültürü ve Ziehl-Neelsen (ZN) ile direkt mikroskopik inceleme yöntemleriyle karşılaştırmalı olarak değerlendirilmesidir. Çalışmaya, tüberküloz şüpheli hastalara ait 50 balgam, 25 bronkoalveoler lavaj, beş torasentez sıvısı ve beş idrar olmak üzere toplam 85 örnek dahil edilmiştir. Tüm örnekler dekontamine edilmiş ve çalışmalar Xpert MTB/RIF hariç, dekontamine örnek süspansiyonundan gerçekleştirilmiştir. Çalışmamızda incelenen 85 örneğin 25 (%29)'inde Bactec 460TB, 25 (%29)'inde Xpert MTB/RIF, 15 (%18)'inde LJ ve 11 (%13)'inde ZN boyama yöntemi ile pozitif sonuç elde edilmiştir. Bactec 460TB sonuçları referans olarak alındığında, Bactec 460TB ile Xpert MTB/RIF arasında anlamlı olarak yüksek düzeyde korelasyon saptanmıştır (r= 0.943, p= 0.000). Referans teste göre Xpert MTB/RIF sistemi ile bir örnekte yanlış pozitiflik belirlenmiş ve Xpert MTB/RIF testinin duyarlılık, özgüllük, pozitif ve negatif öngörü değerleri sırasıyla %96, %98, %96 ve %98 olarak hesaplanmıştır. Çalışma kapsamında izole edilen suşlar için direnç saptanmamıştır. Bu çalışma ile Xpert MTB/RIF sisteminin mikroskopi negatif ve pozitif örnekler için referans testle benzer duyarlılığa sahip olduğunu destekleyen veriler elde edilmiştir. Ayrıca, Xpert MTB/RIF sonuçlarının iki saatten kısa zamanda alınmasının önemli bir avantaj olduğu düşünülmüştür.
Anahtar sözcükler: Mycobacterium tuberculosis; Xpert MTB/RIF; Bactec 460TB; Löwenstein Jensen.
ABSTRACT
Tuberculosis is still a major global health problem. Nowadays nucleic acid amplification tests which are recommended by the World Health Organization (WHO) become popular methods for the rapid detection of Mycobacterium tuberculosis complex (MTC). Recently introduced commercial Xpert MTB/RIF (Cepheid, USA) system is also a molecular method based on real-time polymerase chain reaction for simultaneous detection of both MTC and rifampicin resistance in the clinical sample. The sample processing, nucleic acid extraction, amplification and detection of known mutations related to rifampicin resistance are performed in a single cartridge in this integrated system and the results are obtained in two hours. The aim of this study was to evaluate the performance of Xpert MTB/RIF system for the detection of M.tuberculosis in pre-processed clinical samples by comparing the results obtained by Bactec 460TB 12B (BD Diagnostic, USA), Löwenstein-Jensen (LJ) culture and direct microscopy of smears stained with Ziehl-Neelsen (ZN). A total of 85 clinical specimens (50 sputum, 25 bronchoalveolar lavage, five thorasynthesis fluid and five urine samples) obtained from tuberculosis-suspected patients were included to the study. All specimens were decontaminated and this decontaminated suspension was used in the diagnostic methods, except for Xpert MTB/RIF process. Twenty-five (29%) of the samples yielded positive result with Bactec 460TB, 25 (29%) were found positive with Xpert MTB/RIF, 15 (18%) were found positive with LJ and 11 (13%) were found positive with ZN staining method. High consistency was detected between the results of Bactec 460TB and Xpert MTB/RIF when Bactec 460TB was considered as the gold standard method (r= 0.943; p= 0.000). One specimen yielded false positive result with Xpert MTB/RIF when compared to the reference method. The sensitivity, specificity, positive and negative predictive values of Xpert MTB/RIF test were then estimated as 96%, 98%, 96% and 98%, respectively. No resistance were detected for the tested isolates. This study suggested that the sensitivity of Xpert MTB/RIF system in direct detection of M.tuberculosis in smear positive and smear negative samples was consistent with the reference methods. Moreover, the MTB/RIF test provided sensitive detection of tuberculosis in less than two hours.
Key words: Mycobacterium tuberculosis; Xpert MTB/RIF; Bactec 460TB; Löwenstein Jensen.
Geliş Tarihi (Received): 04.06.2010 • Kabul Ediliş Tarihi (Accepted): 23.11.2010
GİRİŞ
Tüberküloz, yılda yaklaşık sekiz milyon yeni olgunun ortaya çıkması nedeniyle, halen temel bir sağlık problemi olmaya devam etmektedir1. Hastalığın yayılımının azaltılmasında, hızlı ve doğru laboratuvar tanısı önemli bir yere sahiptir2. Dünya Sağlık Örgütü (DSÖ), klinik örneklerden Mycobacterium tuberculosis'in izolasyonu, tanımlanması ve ilaçlara karşı duyarlılıklarının belirlenerek sonuçların en geç üç hafta içinde alınmasını önermektedir. Mevcut klasik yöntemlerle testleri bu sürede sonuçlandırmak olanaklı görülmemektedir3. Bu nedenle yeni moleküler biyolojik yöntemlerin kullanılması, problemin çözümüne katkı sağlayabilir4,5. Nükleik asit amplifikasyon testleri (NAT)'nin tamamında örnek hazırlama, nükleik asit saflaştırması, amplifikasyon ve sonuç değerlendirme işlemleri ayrı ayrı yapılmaktadır6. Konvansiyonel NAT zaman kaybına, iş yükünün artmasına ve bazen de gereksiz harcamalara neden olmaktadır.
Günümüzde, tüberküloz basillerinin tanısı ve ilaç direncinin belirlenmesinde kullanılan moleküler testler için önemli gelişmeler söz konusudur. Özellikle yarı kantitatif nested gerçek zamanlı polimeraz zincir reaksiyonu (PCR) temeline dayanan "Xpert MTB/RIF" (Cepheid, ABD) yönteminin, M.tuberculosis kompleks ve rifampisin direncini doğrudan hasta örneğinden bir tek çalışma ile iki saatten kısa sürede saptayabildiği ifade edilmektedir7. Bu çalışmada, tüberküloz şüpheli hastalardan alınan örneklerde M.tuberculosis varlığının saptanmasında Xpert MTB, direkt mikroskopik inceleme, Bactec 460TB ve Löwenstein-Jensen kültür yöntemleri ile yapılan çalışmalar sonucu elde edilen verilerin karşılaştırılması amaçlanmıştır.
GEREÇ ve YÖNTEM
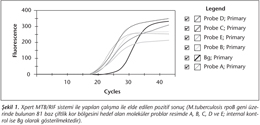
Çalışmaya, laboratuvarımıza gönderilen tüberküloz şüpheli hastalara ait 50 balgam, 25 bronkoalveoler lavaj, beş torasentez sıvısı ve beş idrar olmak üzere toplam 85 örnek dahil edildi. Moleküler çalışmalar için örneklere homojenizasyon ve dekontaminasyon işlemi uygulanmadı. Örnek ve aktarma solüsyonu (Pour Sample Reagent) 1/1 oranında 1.5 ml'lik steril santrifüj tüplerine alındıktan sonra 15 dakika oda sıcaklığında inkübe edildi. Kit içeriğinde gelen steril pastör pipeti ile, karışımdan gerekli miktar alınıp aerosol oluşumuna engel olmak amacıyla yavaşça test kartuşuna aktarılıp kapağı kapatıldı. Birkaç dakikada gerçekleştirilen ön işlemler sonrası hazırlanan kartuş GeneXpert (Cepheid GeneXpert® System, ABD) cihazına yerleştirilip sistem çalıştırıldı8. Sonuçlar iki saat içinde alındı (Şekil 1).
Bactec 460TB (BD Diagnostic, ABD) ve konvansiyonel yöntemler için örneklere homojenizasyon ve dekontaminasyon işlemleri uygulandı. Örnekler, Ziehl-Neelsen (ZN) yöntemi ile boyanarak aynı gün mikroskobik olarak incelendi ve ayrıca Löwenstein-Jensen (LJ) besiyerine ekimleri yapıldı. LJ için üreme kontrolü, gözle değerlendirme ve kültürden ZN yöntemi ile boyanarak yapıldı. Bactec 460TB 12B (Middlebrook 7H12 Medium) şişelerine ekimi takiben yapılan okumalarda, uygun büyüme indeksi (growth index) artışını gösteren örnekler, üretici firma önerileri doğrultusunda tanımlama ve ilaç direnci çalışmalarına alındı.
Değişkenler arasındaki ilişkinin saptanması amacıyla Pearson korelasyon analizleri SPSS 17.0 programı kullanılarak gerçekleştirildi.
BULGULAR
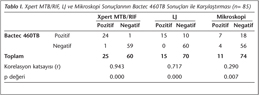
Çalışmada incelenen 85 örneğin 25 (%29)'inde Bactec 460TB, 25 (%29)'inde Xpert MTB/RIF, 15 (%18)'inde LJ ve 11 (%13)'inde ZN boyama yöntemi ile pozitif sonuç elde edilmiştir. Bactec 460TB sonuçları referans olarak alındığında, Bactec 460TB ile Xpert MTB/RIF arasında anlamlı olarak yüksek düzeyde korelasyon (r= 0.943) saptanmıştır. Bactec 460TB ile LJ sonuçları arasında da anlamlı bir korelasyon (r= 0.717) belirlenmiştir (Tablo I).
Bactec 460TB sonuçları referans olarak kabul edilerek, mevcut sınırlı verilerle yapılan istatistiksel analizlerde Xpert MTB/RIF testinin özgüllüğü 0.98, duyarlılığı 0.96, pozitif öngörü değeri 0.96 ve negatif öngörü değeri 0.98 olarak hesaplanmıştır.
Çalışma kapsamında izole edilen suşlar için direnç saptanmamıştır.
TARTIŞMA
Ticari bir sistem olan Xpert MTB/RIF, M.tuberculosis'in rpoB geni üzerinde bulunan 81 baz çiftlik kor (core) bölgesini hedef alan moleküler problar (beacons) içermektedir. Bu problar sayesinde rifampisin (RIF)'e dirençli suşların %95'inde gözlenen mutasyonlar da saptanabilmektedir. Prob tasarımı RIF direnci ile ilişkili mutasyonların araştırılmasını mümkün kılmaktadır. Xpert MTB/RIF, bütünleşik bir yapıya sahip olup, örneklerin işlenmesi birkaç dakikada sonlandırılmakta ve sistem gerçek zamanlı PCR temeli ile çalışmaktadır. Nükleik asit izolasyonu, amplifikasyon ve mutasyon saptama işlemleri tek bir kartuş içerisinde gerçekleşmektedir. Üretici firma tarafından Xpert MTB/RIF sistemi ile bakteri varlığının saptanmasında alt sınır, 131 koloni oluşturan birim (kob)/ml olarak bildirilmektedir. Ayrıca, sistem RIF direncinden yaygın olarak sorumlu olan 23 farklı mutasyonun test edilmesine olanak sağlamaktadır. Helb ve arkadaşları9 tarafından yapılan bir çalışmada, mikroskopi ve kültür pozitif örneklerde Xpert MTB/RIF yönteminin duyarlılığı %100 (29/29); mikroskopi negatif, LJ pozitif örnekler için ise %84.6 (33/39) olarak bildirilmiştir. Bu testin, mikroskopi negatif, LJ ve sıvı besiyeri pozitif örnekler için %71.7 oranında pozitiflik saptadığı ve kültür negatif örneklerin hiçbirinde M.tuberculosis için pozitif sonuç vermediği gösterilmiştir. Önceden tedavi görmüş hastalara ait, mikroskopi ve kültür pozitif örneklerin %98.4 (63/64)'ünden, bu yöntemle iki saat gibi kısa bir sürede pozitif sonuç alındığı da vurgulanmıştır9.
Kültür ve Xpert MTB/RIF sonuçlarının karşılaştırıldığı bir başka çalışmada, duyarlılık %90.3, özgüllük %99.7, pozitif öngörü değeri %96.5, negatif öngörü değeri ise %99.3 olarak bulunmuş; Xpert MTB/RIF pozitifliklerinin %24'ünün mikroskopi negatif örneklere ait olduğu ifade edilmiştir10. Kültür ve Ziehl-Neelsen (ZN) boyama ile pozitif direkt örneklerden yapılan bir çalışmada da, özgüllüğün %99.2, duyarlılığın %98.6 olduğu, ZN boyama ile negatif, kültür pozitif direkt örnekler için ise duyarlılığın %90.2 olduğu bildirilmiştir11.
Çalışmamız kapsamında, Bactec 460TB sonuçlarının referans olarak alınmasıyla gerçekleştirilen istatistiksel analizlerde Bactec 460TB ve Xpert MTB/RIF arasında yüksek düzeyde korelasyon saptanmıştır. Bactec 460TB ile negatif sonuç veren bir örnekte Xpert MTB/RIF sistemi ile pozitiflik saptanması dikkat çekici bulunmuş; Bodmer ve arkadaşlarının10 yaptıkları çalışmada da, kültür negatif bir örnek için Xpert MTB/RIF ile pozitiflik saptandığı belirlenmiştir.
Xpert MTB/RIF yönteminin olumlu yönleri arasında, hızlı ve kolay uygulanabilir olması; mikroskopi negatif, kültür pozitif örneklerin çoğunda pozitif sonuç vermesi; RIF direnci ile ilişkili olduğu bilinen mutasyonları yüksek duyarlılıkta saptayabilmesi; gereken tüm reaktiflerin kapalı bir kartuşta bulunması ve internal kontrol ihtiva etmesi sayılabilir. Ancak yöntemin henüz deneme aşamasında olması, ulaşılabilir kaynaklardaki verilerin oldukça sınırlı ve yöntemin pahalı olması olumsuz yönleri olarak vurgulanabilir. Bu itibarla Xpert MTB/RIF sistemi ile çalışmalar planlanırken maliyet-etkinlik analizleri ayrıntılı olarak yapılmalıdır.
KAYNAKLAR
- American Thoracic Society. Diagnostic standards and classification of tuberculosis in adults and children. Am J Respir Crit Care Med 2000; 161(4): 1376-95. [Tam Metin] [PDF]
- Cesur S, Hoca NT, Tarhan G, et al. Evaluation of Quantiferon-TB Gold and tuberculin skin test in patients with tuberculosis, close contact of patients, health care workers and tuberculosis laboratory personnel. Mikrobiyol Bul 2010; 44(4): 553-60. [Özet]
- Kıyan M. Mycobacteriaceae, s: 419-57. Cengiz AT, Ustaçelebi Ş (ed), Temel ve Klinik Mikrobiyoloji. 1999, Güneş Kitabevi, Ankara.
- Esen N, Özkütük A, Çoban H, Atlas E. Three step MIRU-VNTR for routine mycobacteriology laboratory practice. Mikrobiyol Bul 2010; 44(3): 375-83. [Özet]
- Seber E. Tüberküloz laboratuvar tanı yöntemleri: Löwenstein Jensen besiyeri ile antitüberküloz duyarlılık testi (Modifiye orantılama dilüsyon testi), s: 467-76. 21. Yüzyılda Tüberküloz Sempozyumu ve 2. Tüberküloz Laboratuvar Tanı Yöntemleri Kursu Kitabı. 2003, Klimik ve Toraks Derneği, İstanbul.
- Kwara A, Schiro R, Cowan LS, et al. Evaluation of the epidemiologic utility of secondary typing methods for differentiation of Mycobacterium tuberculosis isolates. J Clin Microbiol 2003; 41(6): 2683-5. [Özet] [Tam Metin] [PDF]
- Durmaz R. Mycobacterium tuberculosis suşlarında direncin belirlenmesinde moleküler yöntemler: Son gelişmeler. ANKEM 2010; 24 (Ek 2): 64-70. [PDF]
- http://www.cepheidinternational.com/tests-and-reagents/ce-ivd-test/xpert-mtbrif/
- Helb D, Jones M, Story E, et al. Rapid detection of Mycobacterium tuberculosis and rifampin resistance by use of on-demand, near-patient technology. J Clin Microbiol 2010; 48(1): 229-37. [Özet] [Tam Metin] [PDF]
- Bodmer T, Ströhle A. Diagnosing pulmonary tuberculosis in a low prevalence setting-the Xpert MTB/RIF test. 20th European Congress of Clinical Microbiology and Infectious Diseases (ECCMID), 10-13 April 2010, Vienna, Austria. P2048.
- Boehme CC, Nabeta P, Hillemann D, et al. Rapid molecular detection of tuberculosis and rifampin resistance. N Engl J Med 2010; 363(11): 1005-15. [Özet] [Tam Metin] [PDF]
İletişim (Correspondence):
Doç. Dr. İhsan Hakkı Çiftçi,
Afyonkarahisar Üniversitesi Tıp Fakültesi,
Tıbbi Mikrobiyoloji Anabilim Dalı,
03100, Afyonkarahisar, Türkiye.
Tel (Phone): +90 505 274 7077,
E-posta (E-mail): ihciftci@hotmail.com